
| A. | 3Cl2+6FeI2═4FeI3+2FeCl3 | B. | 3Cl2+2FeI2═2FeCl3+2I2 | ||
| C. | Co2O3+6HCl═2CoCl2+Cl2↑+3H2O | D. | 2Fe3++2I-═2Fe2++I2 |
分析 根据化学方程式,只要根据氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性得出的结果符合题干已知条件的,说明反应成立.
解答 解:A、根据反应:3Cl2+6FeI2=2FeCl3+4FeI3,得出氧化性是:Cl2>FeCl3,但是氧化性是FeCl3>I2,还原性是碘离子强于亚铁离子,碘离子会先被氯气氧化,和题意不相符合,不可能发生,故A错误;
B、因为氧化性FeCl3>I2,所以氯气先氧化碘离子后氧化铁离子,故B正确;
C、根据反应:Co2O3+6HCl=2CoCl2+Cl2↑+3H2O,得出氧化性是:Co2O3>Cl2,和题意相符合,反应可能发生,故C正确;
D、因为氧化性FeCl3>I2,所以2Fe3++2I-=2Fe2++I2能发生,故D正确;
故选A.
点评 本题考查学生分析和解决问题的能力,可以根据氧化剂的氧化性大于氧化产物的氧化性,难度不大.


科目:高中化学 来源: 题型:选择题
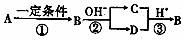 化合物A、B、C、D中均含有短周期元素X,B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是
化合物A、B、C、D中均含有短周期元素X,B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是| A. | X元素可能是金属,也可能是非金属 | |
| B. | 反应①、②、③均为氧化还原反应 | |
| C. | 反应②、③为可逆反应 | |
| D. | 若B为金属单质,反应①的“一定条件”为电解时,通常加入冰晶石作为助溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

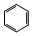 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$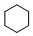
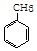 +3HO-NO2$→_{△}^{浓硫酸}$
+3HO-NO2$→_{△}^{浓硫酸}$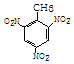 +3H2O,反应类型取代反应
+3H2O,反应类型取代反应 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W<X<Y<Z | |
| B. | 简单氢化物的稳定性:X>Y>Z | |
| C. | W分别与X、Z形成的化合物均能抑制水的电离 | |
| D. | 在化合物A 的分解反应中丙为氧化产物,丁为还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B能形成离子化合物,且A离子半径小于B离子半径 | |
| B. | A、D能形成离子化合物DA5,与H2O反应能生成A的单质 | |
| C. | C、D的简单氢化物中只有D溶于水,其水溶液呈酸性 | |
| D. | E的两种氢化物中所有化学键种类完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
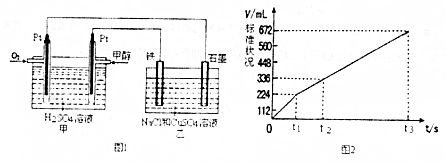
| 容器 | A | B |
| 反应物投入量 | 1molCO2(g)和3molH2(g) | 1molCH3OH(g)和1molH2O(g) |
| 反应能量变化 | 放出29.4KJ | 吸收aKJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 25℃,两片相同的Al片分别和等体积稀HNO3和浓HNO3反应 | 前者产生无色气体,后者产生红棕色气体,且后者反应更加剧烈 | 其他条件相同时,反应物浓度越大,反应速率越快 |
| B | 将无水乙醇和浓H2SO4的混合物加热至170℃,产生的气体通入酸性KMnO4溶液 | KMnO4溶液紫红色褪去 | 乙烯具有还原性 |
| C | SO2通入BaCl2溶液,然后滴入稀硝酸 | 有白色沉淀产生,加入稀硝酸后沉淀不溶解 | 所得沉淀为BaSO3,后转化为BaSO4 |
| D | 向盛有AgCl固体试管中加入一定量的0.01mol•L-1 KI溶液 | 固体由白色逐渐变为黄色 | Ksp(AgCl)>Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 51 | B. | 54 | C. | 57 | D. | 60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com