
【题目】实验室制备1,2二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2===CH2↑+H2O
CH2===CH2↑+H2O
CH2===CH2+Br2→BrCH2CH2Br
可能存在的副反应有乙醇在浓硫酸存在下140℃时脱水生成乙醚。
用少量的溴和足量的乙醇反应制备1,2二溴乙烷的装置如图所示:
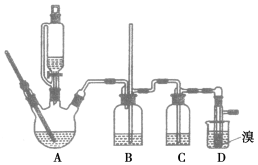
乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
请回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度升高到170℃左右,最主要的目的是________(填序号,下同)。
a.引发反应
b.加快反应速度
c.防止乙醇挥发
d.减少副产物乙醚生成
(2)在装置C中应加入___________,其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸
c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是____________________。
(4)将1,2二溴乙烷粗产品置于分液漏斗中,加水振荡后静置,产物应在________(填“上”或“下”)层。
(5)若产物中有少量未反应的Br2,最好用________洗涤除去。
a.水 b.氢氧化钠溶液
c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用________的方法除去。
(7)反应过程中应用冷水冷却装置D,其主要目的是________________;但又不能过度冷却(如用冰水),其原因是____________________。
【答案】(1)d (2)c (3)溴的颜色完全褪去
(4)下 (5)b (6)蒸馏
(7)避免溴大量挥发 1,2二溴乙烷的熔点低,过度冷却会使其凝固而堵塞导管
【解析】(1)因“乙醇在浓硫酸存在下140℃时脱水生成乙醚”,故需要迅速地把反应温度升高到170℃左右,原因是减少副产物乙醚生成。
(2)因装置C的目的是吸收反应中可能生成的酸性气体,故应选氢氧化钠溶液。
(3)实验是用少量的溴和足量的乙醇反应制备1,2二溴乙烷,反应结束时溴已经反应完,明显的实验现象是溴的颜色完全褪去。
(4)由表中数据可知,1,2二溴乙烷的密度大于水的,因而在下层。
(5)Br2能与氢氧化钠溶液反应,故可用氢氧化钠溶液洗涤;虽然也能与碘化钠溶液反应,但生成的I2会溶于1,2二溴乙烷。
(6)根据表中数据,乙醚的沸点低,可通过蒸馏除去(不能用蒸发,乙醚有毒,不能挥发到空气中)。
(7)溴易挥发,冷水可减少其挥发。但如果用冷水冷却,会使1,2二溴乙烷凝固而堵塞导管。


科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 煤经过气化、液化等物理变化可转变为清洁燃料
B. 棉、麻、丝、有机玻璃都是天然高分子材料
C. 颗粒(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶
D. 青铜、黄铜、碳素钢都属于合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积浓度均为0.1mol/L的三种溶液:①CH3COOH溶液、②HSCN溶液、③NaHCO3溶液混合,①、②分别与③混合,实验测得产生的CO2气体体积(V)随时间(t)的变化如图所示,下列说法正确的是( )
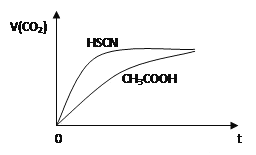
A. 三种溶液pH的比较③>②>①
B. 反应结束后所得两溶液中,c(CH3COO-)>c(SCN-)
C. 上述三种溶液中水电离的电离度:NaHCO3>CH3COOH>HSCN
D. ①与③反应所得的溶液中:c(CH3COO-) + c(CH3COOH) = 0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光纤通信是70年代后期发展起来的一种新型通信技术,目前长距离光纤通信系统已投入使用,光纤通信的光导纤维是由下列哪种物质经特殊工艺制成的
A.石墨 B.石英 C.石灰石 D.高纯硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理揭示了不同的物质在水溶液中有不同的行为。请按要求回答下列问题:(已知:H2SO3: Ka1=1.7×10-2,Ka2=6.0×10-8 ; NH3·H2O:Kb=1.8×10-5)
(1)将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈_________性,该溶液中各离子浓度由大到小的顺序为:_______________,所得溶液中c(H+)-c(OH-)=_______________(填写表达式)
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。
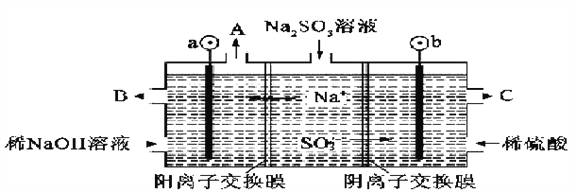
①图中a极要连接电源的(填“正”或“负”)________极;C口流出的物质是________。
②![]() 放电的电极反应式为_______________。
放电的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,钴氧化物可通过处理钴渣获得。
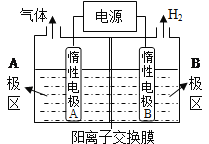
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.B极区电解液为 溶液(填化学式),阳极电极反应式为 ;电解过程中Li+向 电极迁移(填“A”或“B”)。
(2)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:

Co(OH)3溶解还原反应的离子方程式为 ,铁渣中铁元素的化合价为 ,在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不用其他试剂,用最简单的方法鉴别下列物质:( )
①NaOH溶液,②Mg(NO3)2溶液,③CuSO4溶液,④KCl溶液,正确的鉴别顺序是
A. ①②③④ B. ③④②①
C. ④①②③ D. ③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如图所示(部分产物已略去):

(1)写出用惰性电极电解M溶液的离子方程式____________。
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是__________________。
(3)若A是CO2气体,A与B溶液反应后所得的溶液再与盐酸反应,放出气体的物质的量与所加盐酸体积之间的关系如下图所示,“则A与B溶液”反应后溶液中的溶质为__________(填化学式)。
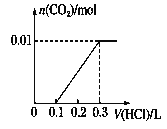
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所能观察到的实验现象是____________________。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚后溶液显紫色,则由A转化成E的离子方程式是_______________ ;
(6)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄露,请写出足量E与D反应的化学方程式___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com