
| A. | CH2═CH-CH═CH2 | B. | HC≡C-CH3 | C. | CH3-C≡C-CH3 | D. | CH2═CH-CH3 |
分析 根据1mol某链烃最多能和2molHCl发生加成反应,则分子中含有2个C=C键或1个C≡C,1mol该卤代烷能和6molCl2发生取代反应,说明1个卤代烷中引入6个Cl原子,加成时1个某链烃分子已引入2个Cl原子形成卤代烷,所以1个最后的有机化合物中分子共含有8个Cl原子,以此来解答.
解答 解:1mol某链烃最多能和2molHCl发生加成反应,则分子中含有2个C=C键或1个C≡C,1个某链烃分子已引入2个Cl原子形成卤代烷;1mol该卤代烷能和6molCl2发生取代反应,说明1个卤代烷中引入6个Cl原子,所以最后的有机化合物1个分子含有8个Cl原子,则C原子数目为3,故该烃的分子式为为C3H4,
故选B.
点评 本题考查有机物的推断,明确加成反应与取代反应的实质是解答本题的关键,注意1mol该卤代烷能和6molCl2发生取代反应,说明1个卤代烷中引入6个Cl原子.


科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 不断补充氮气 | ||
| C. | 增大压强 | D. | 及时将NH3从密闭容器中转移走 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2b+n-8ROb | B. | HnROb | C. | H8-nROb | D. | H2b-n-8ROb |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
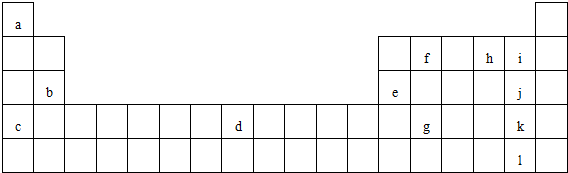
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用红外光谱法鉴别乙醇和二甲醚 | |
| B. | 用酸性高锰酸钾溶液鉴别乙烷和乙炔 | |
| C. | 用溴水鉴别苯和四氯化碳 | |
| D. | 用溴水鉴别苯和甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
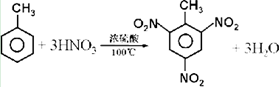
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl稳定性比HI好 | |
| B. | CH4的沸点比NH3的沸点低 | |
| C. | Mg失电子能力比Ca弱 | |
| D. | NaCl与NH4Cl含有的化学键类型完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 电能是现代社会应用最广泛的能源之一.原电池是一种将化学能转化为电能的装置.如图所示的锌、铜和稀硫酸组成的原电池中,锌片上发生氧化反应(填“氧化”或“还原”).铜片上的电极反应式是2H++2e-=H2↑.能否根据反应NaOH+HCl=NaCl+H2O 设计成原电池,否(填“能”或“否”),原因是该反应不是氧化还原反应,没有电子转移.
电能是现代社会应用最广泛的能源之一.原电池是一种将化学能转化为电能的装置.如图所示的锌、铜和稀硫酸组成的原电池中,锌片上发生氧化反应(填“氧化”或“还原”).铜片上的电极反应式是2H++2e-=H2↑.能否根据反应NaOH+HCl=NaCl+H2O 设计成原电池,否(填“能”或“否”),原因是该反应不是氧化还原反应,没有电子转移.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com