
【题目】下列检验方法,利用该气体的氧化性的是
A. Cl2使湿润的淀粉碘化钾试纸变蓝
B. SO2使品红溶液褪色
C. NH3使湿润的红色石蕊试纸变蓝
D. NO遇到空气变为红棕色
科目:高中化学 来源: 题型:
【题目】锂离子电池电极材料钛酸锂Li2Ti5O15含有过氧键(O-O),该化合物中Ti的化合价为+4,则Li2Ti5O15中过氧键的数目为
A. 2个 B. 4个 C. 6个 D. 8个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法不正确的是
A. 用碳酸钠溶液可一次性鉴别乙酸、苯和乙醇三种无色液体
B. ![]() 中所有原子可能共平面
中所有原子可能共平面
C. 1 mol苹果酸(HOOCCHOHCH2COOH)可与3mol NaHCO3发生反应
D. —C3H7和—C2H5O各取代苯分子中的一个氢原子形成的二元取代物的同分异构体有24种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酚酞是白色结晶,在空气中稳定,几乎不溶于水,常用做酸碱指示剂,其结构简式如下图:
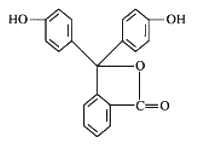
(1)从结构上分析,酚酞可看作____(填序号)。
a.烯烃 b.芳香烃 c.醇类物质 d.酚类物质e.羧酸类物质f.酯类物质
(2)酚酞的分子式为____________。
(3)1个酚酞分子中含有____个饱和碳原子;1mol酚酞可以与_____mol金属钠发生反应。
(4)实验室中常用的酚酞溶液,其溶剂是_______(填“水”、“乙醇”或“四氯化碳”),酚酞可以看作一种弱酸,做指示剂时不能滴加太多,请写出在氢氧化钠溶液中滴加几滴酚酞后的反应方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学做“硫在氧气中燃烧”的实验时,老师建议在集气瓶底部放少量NaOH溶液吸收生成的SO2。这种做法引起了同学们的思考:SO2与NaOH是否发生反应。
【查阅资料】通常状况下,1体积水约能溶解40体积SO2。
【实验方案】同学们向充满SO2的软塑料瓶中迅速倒入一定量NaOH溶液,拧紧瓶盖,振荡,发现塑
料瓶变瘪,他们认为SO2与NaOH发生了反应。
【反思与改进】甲同学认为上述实验不够严谨,理由是_________________。于是同学们设计了如下两
个改进方案。
方案一:
实验操作 | 实验现象 |
向两个充满SO2的200 mL软塑料瓶中分别注入10 mL水和NaOH溶液,振荡,对比。 | 两个瓶子变瘪的程度完全相同 |
乙同学认为由于两个瓶子变瘪的程度完全相同,因此无法证明SO2与NaOH是否发生了反应。试分析导致两个瓶子变瘪的程度完全相同的原因是_____________________。他认为若改变注入水和NaOH溶液的体积便可达到实验目的,注入液体的体积可以是__________(填序号)。
a.15 mL b.8 mL c.5 mL d.3 mL
方案二:
实验操作 | 实验现象 |
利用如图所示装置进行实验: 向两个充满SO2的300 mL集气瓶 中分别加入6 mL水和NaOH溶液, 一段时间后,打开止水夹,对比。
| 倒吸入两个集气瓶中的液体体积完全相同 |
丙同学认为上述方案也无法证明SO2与NaOH是否发生反应。你认为导致吸入液体的体积完全相同的原因是___________________。
丁同学思考后,将上述装置进行了改进,便达到实验目的。改进装置如下图所示,你认为装置B的作用是_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有下列几组物质,请将序号填入下列空格内:
A.CH2=CH-COOH和油酸(C17H33COOH) B.12C60和石墨
C.![]() 和
和 ![]() D.35Cl和37Cl E.乙醇和乙二醇
D.35Cl和37Cl E.乙醇和乙二醇
①互为同位素的是_____________;②互为同系物的是________________;
③互为同素异形体的是__________;④互为同分异构体的是_____________;
⑤既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是____。
(2)写出下列有机物的系统命名或结构简式:
A.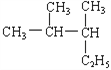 :________________________;
:________________________;
B.CH3CH(CH3)C(CH3)2(CH2)2CH3:_______________________;
C.3,4-二甲基-4-乙基庚烷:______________________________;
D.2-甲基-2-丁烯:_________________;
E.2,4,6-三硝基苯酚:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碳酸钠和碳酸氢钠混合物,取m g固体样品进行加热,完全分解产生CO2112 mL;另取m g固体样品溶于水,向所得溶液中逐滴加入150 mL稀盐酸时产生CO2 112 mL,过量时产生CO2 448 mL(气体体积均为标准状况下测定)。
(1)碳酸氢钠与碳酸钠的物质的量之比为____________________________________________。
(2)盐酸物质的量浓度为______________(保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200mL0.1molL﹣1的Fe(NO3)2溶液中加入适量的NaOH溶液,使Fe2+恰好完全沉淀,过滤,小心加热沉淀,直到水分蒸干,再灼烧到质量不再变化,此时固体的质量为( )
A. 1.44 g B. 1.6 g C. 2.82 g D. 4.36 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有48.4 g碱式碳酸镁样品(化学式:xMgCO3·yMg(OH)2·zH2O,x、y、z为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入150 mL某浓度的盐酸中,充分反应后生成CO2 4.48 L(已折算成标准状况下),所得溶液稀释至250 mL,测得溶液的c(H+)=0.100 mol·L-1。
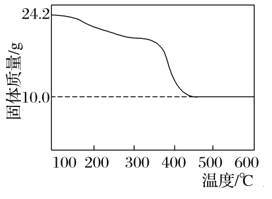
按要求回答下列问题:
(1)盐酸的物质的量浓度c(HCl)=________mol·L-1。
(2)x∶y∶z=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com