
 .
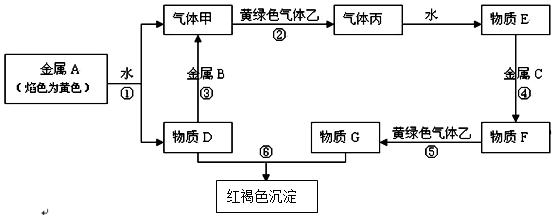
.分析 金属A焰色反应为黄色,故A为金属Na,由反应①可知,D为NaOH,气体甲为H2;氢氧化钠与金属B反应生成氢气,故金属B为Al.黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸.氢氧化钠与物质G反应生成红褐色沉淀是Fe(OH)3,故物质G中含有Fe3+,由转化关系HCl$\stackrel{金属C}{→}$物质F$\stackrel{Cl_{2}}{→}$物质G,可知金属C为Fe,物质F为FeCl2,物质G为FeCl3,结合物质的性质解答该题.
解答 解:(1)由以上分析可知,A为Na,原子结构示意图为 故答案为:
故答案为: ;
;
(2)反应③为铝与氢氧化钠反应生成偏铝酸钠和氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
反应⑤氯化亚铁与氯气反应生成氯化铁,反应离子方程式为:2Fe2++Cl2═2Fe3++2Cl-;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;2Fe2++Cl2═2Fe3++2Cl-;
(3)由以上分析可知,G为FeCl3,则物质G中阳离子的操作方法为取物质G少许于试管中,向其中滴加少量的KSCN溶液,溶液变为血红色(或红色),证明物质G中有Fe3+离子,
故答案为:取物质G少许于试管中,向其中滴加少量的KSCN溶液,溶液变为血红色(或红色),证明物质G中有Fe3+离子;
(4)黄绿色气体乙为Cl2,则实验室制取黄绿色气体乙的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,在该反应中如有0.5molCl2生成,转移的电子的物质的量是1mol,制取完毕,多余的Cl2将用NaOH的水溶液来吸收,其离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;1;Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题是考查物质推断与性质、常用化学用语,难度中等,掌握元素化合物的性质是解题的关键,需要学生熟练掌握元素化合物知识,注意特殊的颜色与特殊反应是推断的突破口.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 不能使酸性高锰酸钾溶液褪色 | |
| B. | 所有原子都在同一平面上 | |
| C. | 能使溴水褪色 | |
| D. | 与HCl在一定条件下能加成只得到一种产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{a+m}^{b+m+n}R$ | B. | ${\;}_{a+m}^{b+a-m}R$ | C. | ${\;}_{a}^{b+a}R$ | D. | ${\;}_{a-m}^{a-m+b}R$ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
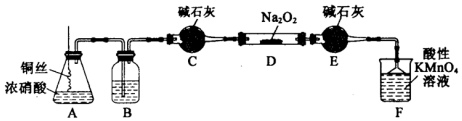
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMn04溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5; 0.1 | B. | 5; 0.2 | C. | 3<x<5; 0.1 | D. | 3<x<5; 0.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
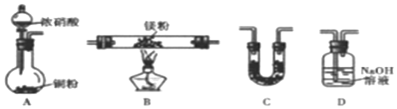
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 实验 | 分离汽油和水 | 通过蒸馏乙醇的水溶 液获得无水乙醇 | 分离 CCl4 中的 I2 | 除去 CO2 气体中的 HCl 气体 |
| 装 置 或 仪 器 | 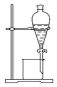 | 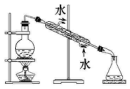 | 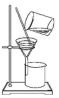 | 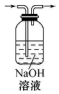 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
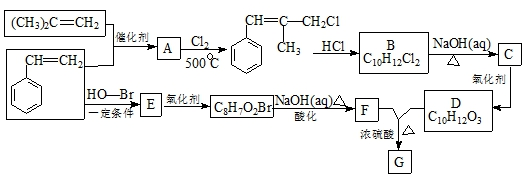
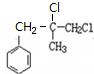 ,B生成C的反应类型为取代反应;
,B生成C的反应类型为取代反应;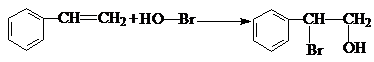 .
.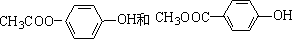 .
. ) 的合成线路:
) 的合成线路: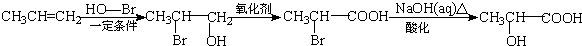 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com