
【题目】化学与生活密切相关.
(1)下列生活用品中,其主要材料属于天然纤维的是_________(填字母序号);
A.塑料保鲜薄 B.橡胶手套 C.棉布围裙
(2)我们常用的洗涤剂清洗餐具上的油污,这是因为洗涤剂具有_________的功能;
(3)食用水果、蔬菜主要补充人体所需的_________;
(4)国家禁止在面粉中添加增白剂过氧化钙CaO2,过氧化钙中氧元素的化合价为_______;
(5)农业上降低土壤酸性的是_________(填化学式);
(6)生活中要用到大量的钢铁,写出赤铁矿(主要成分Fe2O3)冶炼成铁的化学方程式______。
【答案】C 乳化 维生素 -1 Ca(OH)2 3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
【解析】
(1)纤维分为天然纤维和合成纤维,注意区分;
(2)洗涤剂清洗油污后通常形成乳浊液,并非溶液;
(3)水果、蔬菜是人体维生素的重要来源之一;
(4)依据化合价代数和为0判断;
(5)考虑到用碱性物质,氢氧化钙廉价易得;
(6)属于氧化还原反应,注意反应条件的标注;
(1)三大合成材料指的是塑料、合成橡胶和合成纤维。所给三种用品中,塑料和橡胶均是合成材料,棉布的成分是纤维素,是天然纤维,故答案为:C;
(2)洗涤剂是乳浊液,体现了洗涤剂的乳化功能,达到清洗餐具上的油污的目的,故答案为:乳化;
(3)水果、蔬菜中富含维生素,食用水果、蔬菜主要目的之一是补充人体所需的维生素,故答案为:维生素;
(4)过氧化钙中钙元素显+2价,依据元素化合价代数和为0,可以判断出氧元素显-1价,故答案为:-1价;
(5)铝离子和三价铁离子在溶液中水解使土壤显酸性,改良酸性土壤常加入氢氧化钙,使铝离子和三价铁离子转化为磷酸铝和磷酸铁沉淀,达到改良酸性土壤的目的,故答案为:Ca(OH)2;
(5)氧化铁与一氧化碳在高温下反应生成铁和二氧化碳,反应的化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2,故答案为:3CO+Fe2O3
2Fe+3CO2,故答案为:3CO+Fe2O3![]() 2Fe+3CO2。
2Fe+3CO2。


科目:高中化学 来源: 题型:
【题目】实验室欲用氢氧化钠固体配制1.0mol·L-1的氢氧化钠溶液240mL:
(1)配制溶液时,必须用到的玻璃仪器有烧杯、胶头滴管、____________。
(2)计算实验需要称量氢氧化钠的质量为:___________ g
(3)使用容量瓶前必须进行的一步操作是________。
(4)如图是该同学转移溶液的示意图,图中有两处错误,请写出:
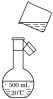
①________________________________________________________________________;
②________________________________________________________________________。
(5)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是______(填字母)。
A.所用氢氧化钠已经潮解
B.向容量瓶中加水未到刻度线
C.有少量氢氧化钠溶液残留在烧杯里
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于四大基本反应类型,但属于氧化还原反应的是
A. 2Na+2H2O===2NaOH+H2↑
B. Cl2+H2O===HCl+HClO
C. CaCO3![]() CaO+CO2↑
CaO+CO2↑
D. Ca(ClO)2+2HCl===CaCl2+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒后驾车是引发交通事故的主要原因之一。酒的主要成分是乙醇。
(1)实验室可用乙醇在一定条件下制得乙烯,写出该反应的化学方程式(要求写反应条件):____。
(2)观察如图制取乙烯和收集装置。请回答:
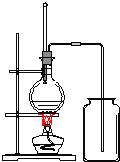
①请指出该装置中两处错误_____,____。
②圆底烧瓶中加入几片碎瓷片的作用是_____。
③写出乙烯使溴水褪色发生反应的化学方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法错误的是( )
A.石油和天然气的主要成分都是碳氢化合物
B.乙酸和乙酸乙酯都能与氢氧化钠溶液反应
C.糖类、油脂和蛋白质都是人体重要的营养物质
D.一定条件下,苯能发生加成反应、取代反应、氧化反应、加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组拟用下图装置制备氢氧化亚铁并观察其颜色。提供化学药品:铁粉、稀硫酸、氢氧化钠溶液。
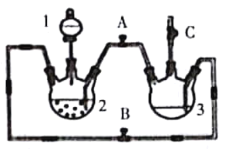
(1)稀硫酸应放在_________中(填写仪器名称).
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关______、打开开关_________就可观察到氢氧化亚铁的颜色。试分析实验开始时排尽装置中空气的理由____________。
(3)该实验使用铁粉,除反应速率可能太快外,还可能会造成的不良后果是_______________。
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](该晶体比一般亚铁盐稳定 ,不易被氧化,易溶于水,不溶于乙醇),用如图所示的装置抽滤,与普通漏斗过滤相比,抽滤的优点是_____________________________。
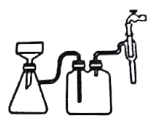
①为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是____。
A.用冷水洗
B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗
D.用90%的乙醇溶液洗
②测定摩尔盐中铁的含量。称取ag产品于锥形瓶中,溶解后加稀硫酸酸化,用c mol·L-1的酸性KMnO4溶液滴定至终点,滴定终点的现象是_______________。到达终点消耗KMnO4的体积为VmL,则该晶体中铁的质量分数的表达式为_______________________(用字母a,c,V 表示)。
③实验室可用______( 填试剂名称)检验Fe2+存在,出现特征蓝色沉淀的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色透明的溶液中:Fe3+、NH4+、I-、CO32-
B.0.1molL-1KNO3溶液中:Na+、Fe2+、Cl-、SO42-
C.使酚酞变红的溶液中:Na+、Mg2+、SO32-、NH4+
D.![]() =1×10-12的溶液:K+、Na+、CO32-、HCO3-
=1×10-12的溶液:K+、Na+、CO32-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3(稀) =3Cu(NO3)2+2NO↑+4H2O
(1)氧化剂是_______,发生氧化反应的物质是__________,被氧化的元素是_______,还原产物是___________.
(2)生成1molNO转移电子_____mol
(3)用单线桥法表示反应电子得失的方向和数目:_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题:
(1)已知分子式为C6H6的有机物有多种,其中的两种为:(Ⅰ)![]() (Ⅱ)
(Ⅱ)![]() 。
。
①这两种结构的区别表现在以下两方面:
定性方面(即化学性质方面):(Ⅱ)能发生的反应___(填字母),而(Ⅰ)不能。
a.被高锰酸钾酸性溶液氧化 b.与溴水发生加成反应
c.与溴发生取代反应 d.与氢气发生加成反应
定量方面(即消耗反应物的量的方面):
1molC6H6与H2加成时:(Ⅰ)需要H2__mol,而(Ⅱ)需要H2__mol。
②今发现C6H6还可能有一种如图![]() 所示的立体结构,该结构的二氯代物有__种。
所示的立体结构,该结构的二氯代物有__种。
(2)如图是制取溴苯的装置,试回答:
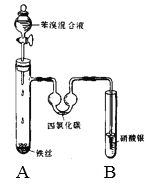
①装置A中发生反应的化学方程式是:____。
②装置B中盛有硝酸银溶液,实验中看到的现象是:___,证明有___生成,说明反应属于___反应(填写反应类型)。
③反应完毕后,将具支试管中的混合液倒入装有水的烧杯中,然后加___溶液后,可除去了其中的溴。写出除溴的化学方程式:___。
④苯易取代,难加成。请写出苯发生硝化反应的方程式:____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com