
【题目】下列说法正确的是( )
A.同温同压下甲烷和氧气的密度之比为2:1
B.1 g甲烷和1 g氧气的原子数之比为5:1
C.等物质的量的甲烷和氧气的质量之比为2:1
D.在标准状况下等质量的甲烷和氧气的体积之比为1:2
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:
【题目】合成氨反应N2(g)+3H2(g)![]() 2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。

请回答下列问题:
(1)该反应通常用铁作催化剂,加催化剂会使图中E变_____(填“大”或“小”),E的大小对该反应的反应热有无影响?________。
(2)起始充入2mol·L-1 N2和5.5 mol·L-1 H2 ,经过50 min,NH3的浓度为1mol·L-1,则v(N2)=_____。
(3)已知NH3(g)= NH3 (l) ΔH=-Q kJ·mol-1,则N2(g)+3H2(g)= 2NH3 (l)的H=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一元银币有银白色的金属光泽,有的同学认为它是由铁制成的,便找磁铁来吸一下,这一过程属于科学探究中的( )
A. 实验 B. 假设 C. 观察 D. 做结论
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等。
①基态Fe3+的M层电子排布式为__________________。
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_________。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于__________(填晶体类型)
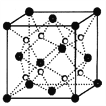
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为__________。已知该晶胞的密度为ρg/cm3,阿伏加德罗常数为NA,求晶胞边长a=__________cm。(用含ρ、NA的计算式表示)
(3)下列说法正确的是__________。
A.第一电离能大小:S>P>Si
B.电负性顺序:C<N<O<F
C.因为晶格能CaO比KCl高,所以KCl比CaO熔点低
D.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大
E.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(4)图1是:Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

①图中d单质的晶体堆积方式类型是______________________。
②图2是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol水_____(填“吸收”或“放出”)的能量是________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为___________________;
(3)在2L的密闭容器中,合成甲醇反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
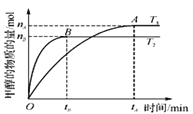
(A、B曲线分别对应T1、T2)
①T1_____T2(填“>”或“ <”)。
②该反应为_____热反应。
③该反应在T1时的平衡常数比T2时的____(填“大”或“小”)。
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)/n(CH3OH)_____。
⑤在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO![]() 2CO2+N2 △H <0。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2 △H <0。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:

请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前2s内的平均反应速率v (N2) = ___________。
②假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是______。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=_____kJ·mol-1。
SO3(g)+NO(g)的ΔH=_____kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=_________。
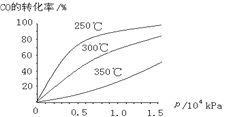
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH_______0(填“>”或“ <”)。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH_______0(填“>”或“ <”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C=2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1molAlN需转移3mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表达正确的是:
A. Na2S2O3溶液与稀H2SO4反应的离子方程式:S2O32- + 6H+ =2S↓ +3H2O
B. H2S的电离方程式:H2S ![]() 2H+ + S2-
2H+ + S2-
C. FeCl3溶液腐蚀印刷电路板的离子方程式:Fe3+ +Cu = Fe2+ + Cu2+
D. HCO3-的电离方程式:HCO3- + H2O![]() CO32- + H3O+
CO32- + H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示的四种实验操作名称从左到右依次是( ) 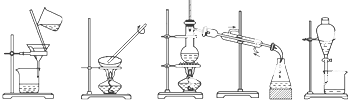
A.过滤、蒸发、蒸馏、分液
B.过滤、蒸馏、蒸发、分液
C.蒸发、蒸馏、过滤、分液
D.分液、蒸馏、蒸发、过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com