
分析 根据n=$\frac{m}{M}$计算出1.7g氨气的物质的量,最高价V=nVm计算出该氨气的体积;氢离子的数目相同,说明二者含有氢原子的物质的量相等,据此进行解答.
解答 解:1.7g NH3的物质的量为:$\frac{1.7g}{17g/mol}$=0.1mol,标准状况下0.1mol氨气的体积为:22.4L/mol×0.1mol=2.24L;
0.1mol氨气分子中含有H原子的物质的量为:0.1mol×3=0.3mol,含有相同数目的氢原子,说明二者含有H的物质的量相等,则需要H2S的物质的量为:$\frac{0.3mol}{2}$=0.15mol,
故答案为:2.24;1.5.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与气体摩尔体积、摩尔质量之间的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的化学计算能力.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:实验题
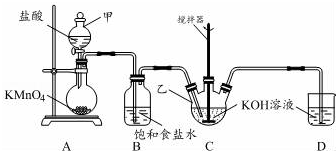 实验室用图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4.
实验室用图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇是一种可再生的绿色能源,CO2是一种温室气体,它们都是重要的化工原料.
甲醇是一种可再生的绿色能源,CO2是一种温室气体,它们都是重要的化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KSCN溶液和氯水 | B. | 铁粉和KSCN溶液 | C. | 浓氨水 | D. | 酸性KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2 化合反应 | |
| B. | CaCO3$\frac{\underline{\;点燃\;}}{\;}$ CaO+CO2↑分解反应 | |
| C. | AgNO3+KCl═AgCl↓+KNO3复分解反应 | |
| D. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
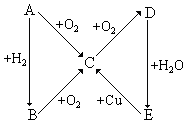 根据如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质和有关反应的化学方程式.
根据如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质和有关反应的化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于同类型反应,化学平衡常数K的大小反映了化学反应可能进行的程度 | |
| B. | 化学反应速率常数k与浓度无关,但受温度、催化剂、固体表面性质等因素的影响 | |
| C. | 水的离子积常数Kw、电离平衡常数Ka与温度有关,不受溶液的酸碱性影响 | |
| D. | 溶度积常数Ksp与难溶电解质的性质和温度无关,只与沉淀的量有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
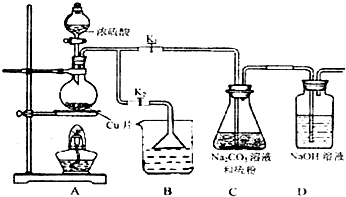
| 编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com