
【题目】下列实验操作合理或能达到实验目的的是
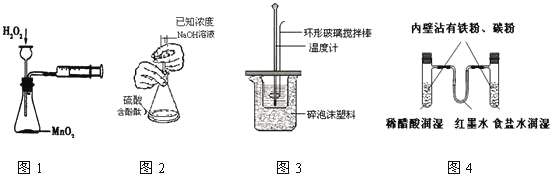
A.图1:实验目的是定量测定化学反应速率
B.图2:用标准NaOH溶液滴定待测H2SO4溶液的物质的量浓度
C.图3:将0.1mol/L 55mLNaOH溶液逐滴加入到0.1mol/L50mL盐酸溶液中测中和热
D.图4:模拟铁的腐蚀实验
科目:高中化学 来源: 题型:
【题目】(1)NH4Cl溶液显_________性,用离子方程式表示原因____________,其溶液中离子浓度大小顺序为_______________________________________。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=________ ,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_________________。
(3)若将等pH、等体积的NaOH和NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m__________n(填“<”、“>”或“=”)。
(4)物质的量浓度相同的NaCl;NaOH;HCl;④NH4Cl;⑤CH3COONa 5种溶液按pH由大到小的顺序为(用④⑤代表相应溶液):_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在密闭容器中发生如下反应2A(g)+B(g)![]() 2C(g),若开始时充入2molC气体,达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2molA和1molB的混合气体,达到平衡时A的转化率为( )
2C(g),若开始时充入2molC气体,达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2molA和1molB的混合气体,达到平衡时A的转化率为( )
A.20%B.40%C.60%D.80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
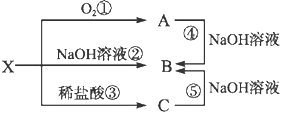
(1)写出以下反应的离子方程式:
②___________________________;
④___________________________。
(2)确定化学式B_______ X_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列说法中正确的是( )

A.1L 1 mol·L-1的醋酸溶液中离子总数为2NA
B.0.05 mol碳酸钠晶体中含离子总数大于0.15NA
C.0.4mol NaCl晶体中含有右图所示的结构单元的数目为0.1NA
D.标准状况下,22.4L CH3Cl和CHCl3的混合物所含有分子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,H2SO3的电离常数:Ka1=1.54×102,Ka2=1×107。向mmL0.1mol/LH2SO3溶液中滴加0.1mol·L1KOH溶液,混合溶液中水电离的c水(H+)与KOH溶液体积V的关系如图所示,下列说法不正确的是

A.m=10
B.c点对应的溶液中存在c(K+)>c(HSO3-)+2c(SO32)
C.b、d两点溶液的pH=7
D.SO32-+H2OHSO3-+OH的K=1×107
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。
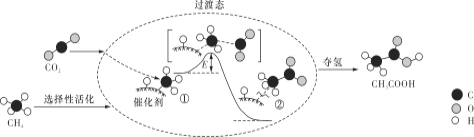
下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行下面的实验要用到下列一种或几种仪器,请用这些仪器的名称填空。
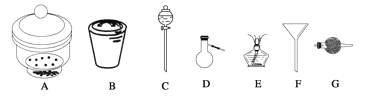
(1)欲干燥NH3需使用仪器_________________________;
(2)欲分离互不相溶的两种液体,可使用____________________________________;
(3)欲分离液态混合物中沸点不同的组分,可使用_____________________________;
(4)欲分离悬浮于液体中的固体物质,可使用_________________________________;
(5)欲用胆矾晶体(CuSO4·5H2O)制无水硫酸铜固体,可使用:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物AX3和单质X2在一定条件下反应可生成化合物AX5。回答下列问题:反应AX3(g)+X2(g)![]() AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。

(1)列式计算实验a从反应开始至达到平衡时的反应速率 v(AX5)=________________。
(2)图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为_______________(填实验序号);与实验a相比,其他两组改变的实验条件是:b_________________、c____________________________________。
(3)用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为_________________;实验a和c的平衡转化率:αa为___________、αc为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com