
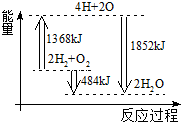
| A.拆开2 mol H2(g)和1 mol O2(g)中的化学键成为H、O原子,共放出1368 kJ能量 |
| B.由H、O原子形成2 mol H2O(g),共吸收1852 kJ能量 |
| C.2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),共吸收484 kJ能量 |
| D.2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 kJ能量 |
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
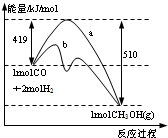 (2010?徐汇区二模)如图是反应CO(g)+2H2(g)→CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
(2010?徐汇区二模)如图是反应CO(g)+2H2(g)→CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO.2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | α 1 | α 2 | α 3 |
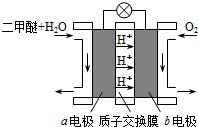
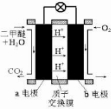 为绿色电源“直接二甲醚燃料电池”工作原理示意图,a电极的反应式为
为绿色电源“直接二甲醚燃料电池”工作原理示意图,a电极的反应式为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com