
 某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.
某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.| Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
| n(Cl-) | 2.5mol | 3.0mol | 4.0mol |
| n(Br-) | 3.0mol | 2.8mol | 1.8mol |
| n(I-) | X mol | 0 | 0 |
| A. | X=0.3 | |
| B. | 溶液中n(Cl-):n(Br-):n(I-)=10:15:4 | |
| C. | 加入的氢氧化钠溶液的浓度为1.45mol•L-1 | |
| D. | 溶液中大量存在的离子共有六种 |
分析 探究一:开始加入20mLNaOH无沉淀生成说明发生的反应是:H++OH-═H2O,则溶液中含有H+,所以不含有CO32-、AlO2-;再加入氢氧化钠溶液至50mL,由图象分析可知生成沉淀增多至最大,反应为Al3++3OH-═Al(OH)3↓,则溶液中含有Al3+;继续加入氢氧化钠,沉淀量不变,说明氢氧化钠和溶液中的铵根离子反应,NH4++OH-?NH3•H2O,则溶液中含有NH4+;消继续加入氢氧化钠溶液,沉淀开始溶解,到加入90mL氢氧化钠溶液,沉淀全部溶解,发生的反应为Al(OH)3+OH-═AlO2-+H2O,消耗氢氧化钠10mL,则溶液中不含有Ag+、Mg2+、Fe3+,在酸性条件下NO3-能氧化碘离子,所以不能含有NO3-;
探究二:还原性:I->Br-,加入氯气5.6L时溶液中I-amol,则说明通入5.6L Cl2只发生:Cl2+2I-═I2+2Cl-,5.6L变成11.2L,消耗5.6L Cl2的物质的量为$\frac{5.6L}{22.4L/mol}$=0.25mol,发生:Cl2 +2Br-═Br2+2Cl-,Cl2+2I-═I2+2Cl-,根据反应方程式计算.
解答 解:探究一:开始加入20mLNaOH无沉淀生成说明发生的反应是:H++OH-═H2O,则溶液中含有H+,所以不含有CO32-、AlO2-;再加入氢氧化钠溶液至50mL,由图象分析可知生成沉淀增多至最大,反应为Al3++3OH-═Al(OH)3↓,则溶液中含有Al3+;继续加入氢氧化钠,沉淀量不变,说明氢氧化钠和溶液中的铵根离子反应,NH4++OH-?NH3•H2O,则溶液中含有NH4+;消继续加入氢氧化钠溶液,沉淀开始溶解,到加入90mL氢氧化钠溶液,沉淀全部溶解,发生的反应为Al(OH)3+OH-═AlO2-+H2O,消耗氢氧化钠10mL,则溶液中不含有Ag+、Mg2+、Fe3+,不能确定是否含有NO3-;
探究二:还原性:I->Br-,加入氯气5.6L时溶液中I-amol,则说明通入5.6L Cl2只发生:Cl2+2I-═I2+2Cl-,5.6L变成11.2L,消耗5.6L Cl2的物质的量为$\frac{5.6L}{22.4L/mol}$=0.25mol,发生:Cl2 +2Br-═Br2+2Cl-,Cl2+2I-═I2+2Cl-,
A.5.6L变成11.2L,消耗Cl2的物质的量为0.25mol,发生:Cl2 +2Br-═Br2+2Cl-,Cl2+2I-═I2+2Cl-,Br-减少0.2mol,则Br-与反应的氯气为0.1mol,所以与反应的氯气为0.15mol,则I-的物质的量为0.3mol,即X=0.3,故A正确;
B.根据表数据:5.6L变成11.2L,消耗Cl2的物质的量为0.25mol,发生:Cl2 +2Br-═Br2+2Cl-,Cl2+2I-═I2+2Cl-,Br-减少0.2mol,则Br-与反应的氯气为0.1mol,所以与反应的氯气为0.15mol,则I-的物质的量为0.3mol,所以原溶液中:n(I-)=0.5mol+0.3mol=0.8mol,n(Cl-)=2.5mol-0.5mol=2mol,n(Cl-):n(Br-):n(I-)=2:3:0.8=10:15:4,故B正确;
C.图象中只有氢氧化钠的体积一种数据无法计算氢氧化钠的浓度,故C错误;
D.溶液中一定含有的离子为Cl-、Br-、I-、H+、Al3+、NH4+,所以溶液中大量存在的离子共六种,故D正确.
故选C.
点评 本题考查离子的判断和计算,图标数据分析的方法和反应实质,题目难度中等,注意根据离子的还原性以及表中数据判断反应的程度,结合方程式计算.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;
 +2C2H5OH$→_{△}^{浓硫酸}$
+2C2H5OH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O. 与足量NaOH溶液反应的化学方程式为
与足量NaOH溶液反应的化学方程式为 .
. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

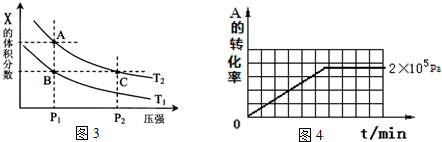
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁发生电化学腐蚀时,负极发生的反应是:Fe-3e-═Fe3+ | |
| B. | 将钢铁与电源的正极相连,可防止钢铁被腐蚀 | |
| C. | 在镀件上镀铜时纯铜作阴极 | |
| D. | 钢铁腐蚀中,吸氧腐蚀比析氢腐蚀更普遍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com