
���ж���Ӧ�л����������ȫ��ȷ���ǣ� ��
�ټ��飺��Ȼ������Ҫ�ɷ֣��ܷ���ȡ����Ӧ������ϩ������һ������ʯ�ͻ�����չˮƽ�ı�־�����Է����ӳɷ�Ӧ���۱���ƽ��ṹ��ÿ�������к���3��̼̼˫��������֬�����ڸ߷��ӻ�������Է���ˮ�ⷴӦ���ݵ��ۣ������������ʣ�����Ԫ�ر���ɫ�������ʣ���Ũ�����Ի�ɫ��ˮ������ղ���Ϊ������
A���٢ڢ� B���ڢܢ� C���٢ݢ� D���٢ڢ�
 �������Ͽ��㱾ϵ�д�
�������Ͽ��㱾ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ�����и߶���9���¿���ѧ�Ծ��������棩 ���ͣ������
���õ���ʽ��ʾ���л�������γɹ���
MgCl2 H2S Na2O H2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ��������У�߶���ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
���й���CH4��H2��C������Դ���ʵ��о�������е��ǣ� ��
A������ˮ����������ǿ���ȼ�յ����ʣ���˿��о���ˮ���ֽ�������ʹ���Ϊ������Դ
B��Ѱ�����ʴ�����ʹCO2��H2O��Ӧ����CH4��O2�����ų�����
C��Ѱ�����ʴ���������̫����ʹ�����е�CO2�ͺ����ɵ�CH4�ϳɺϳ�����CO��H2��
D������̬̼�ϳ�C60����C60��ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ�߶���ѧ��9�µ��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ݵ���������Ӧ���Ȼ�ѧ����ʽ
(i)I2(g)+H2(g) 2HI(g) ��H= - 9.48kJ/mol
2HI(g) ��H= - 9.48kJ/mol
(ii) I2(s)+H2(g) 2HI(g) ��H= + 26.48kJ/mol�������ж���ȷ���� �� ��
2HI(g) ��H= + 26.48kJ/mol�������ж���ȷ���� �� ��
A��254gI2(g)��ͨ��2gH2(g)����Ӧ����9.48kJ
B��1mol��̬����1mol��̬���������������l7.00kJ
C����Ӧ(i)�IJ���ȷ�Ӧ(ii)�IJ����ȶ�
D����Ӧ(i)��1molI-I����1molH-H����Ҫ��������С�ڲ�2molH-I����Ҫ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ�߶���ѧ��9�µ��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������Т�K2SO4 ��HCHO ��MgSO4 ��Hg(NO3)2 ��NH4 Cl ��KOH����ʹ�����ʱ��Ե��� �� ��
Cl ��KOH����ʹ�����ʱ��Ե��� �� ��
A���ڢܢ� B���٢ۢ� C���٢ڢ� D���ܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ�߶����ڳ����Ի�ѧ���������棩 ���ͣ������
��һ���������ܱ������м���2mol A��0.6mol C��һ������B�������壮һ�������·�����Ӧ��������Ũ����ʱ��仯��ͼһ��ʾ��ͼ��Ϊt2ʱ�̺�ı䷴Ӧ������ƽ����ϵ�з�Ӧ������ʱ��仯����������ĸ��ζ����ı�һ�ֲ�ͬ����������֪t3��t4��ʹ���˴�����ͼһ��t0��t1��c��B��δ������

��1����t1=15min����t0��t1����CŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊv��C��=______________��
��2��t4��t5�θı������Ϊ______________��B����ʼ���ʵ���Ϊ______________��
��3���ж�ͼһ�п��淴Ӧ�ﵽƽ��״̬�������ǣ�����ţ�______________��
��2v����A��=3v�棨C��
�ڻ��������ܶȲ���
�ۻ�������ƽ����Է�����������
��A��B��C��Ũ�ȶ����ٷ����仯
��4��t5��t6�α����������¶Ȳ��䣬��A�����ʵ������仯��0.01mol�����˹����������������Ƚ�������Ϊa kJ��д�����¶��¸÷�Ӧ���Ȼ�ѧ����ʽ��______________��
��5���������������������ͬ�ұ��ֲ��䣬�����������¶Ⱥ㶨Ϊ������t4��t5ʱ���¶ȣ���ҪʹC��ƽ��Ũ��Ϊ1.2mol/L�������������м���1.2molA��0.6molB��ͬʱ����Ҫ����___________molC��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ�߶����ڳ����Ի�ѧ���������棩 ���ͣ�ѡ����
��˹�����������Ϳ�ѧ�о����к���Ҫ�����塣��֪3.6g̼��6.4g������ȼ�գ�����Ӧ��ľ����ų���X kJ��������֪̼��ȫȼ�յ��ʱ��H= һY kJ��mol-1����lmol C��O2��Ӧ����CO�ķ�Ӧ�ȡ�HΪ ( ) kJ��mol-1
A��һY B����(10X��Y) C��һ(5X��O.5Y) D��+(10X��Y)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡ�߶��Ͽ�ѧ�⻯ѧ���������棩 ���ͣ������
��һ��������ܱ������У��������»�ѧ��Ӧ��CO(g)+H2O(g) 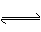 CO2(g)+H2(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO2(g)+H2(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=__________,�÷�ӦΪ__________��Ӧ�������Ȼ���ȣ������ı�����ʹƽ��������Ӧ�����ƶ�����ƽ�ⳣ��_____________������ţ�
��һ������ ��һ����С �ۿ������� ������С��������п���
��2�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������___________��
��a��������ѹǿ���� ��b�����������c��CO������
��c��v��(H2)=v��(H2O) ��d��c��CO��=c��CO2��
��3�� ����ͬ����CO (g) ��H2O (g) �ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������У����з�ӦCO (g) �� H2O (g) CO2 (g) �� H2 (g)���õ�����������
CO2 (g) �� H2 (g)���õ����������� �ݣ�
�ݣ�
ʵ���� | �¶�/�� | ��ʼ | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
H2O | CO | CO2 | CO | |||
A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
C | 900 | a | b | c | d | t |
��ʵ��A���Ԧ�(H2) ��ʾ�ķ�Ӧ����Ϊ ��
��ͨ�������֪��CO��ת����ʵ��A ʵ��B(����ڡ��������ڡ���С�ڡ�)���÷�Ӧ������ӦΪ ��������š����ȷ�Ӧ��
����ʵ��CҪ�ﵽ��ʵ��B��ͬ��ƽ��״̬����a��bӦ����Ĺ�ϵ�� ���ú�a��b����ѧʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ�߶���9.4�ܿ���ѧ���������棩 ���ͣ�ѡ����
���б������ж���ȷ���ǣ� ��
A��25��ʱ��pH��10��NaOH��Һ��pH =10�İ�ˮ�У�c(Na+)=c(NH4+)��
B����ͬ�����µ����ʵ���Ũ�ȵĢ�NaCl��Һ����NaOH��Һ����HCl��Һ����ˮ�������c(H+) ���ۣ��٣���
C����Na2CO3��NaHC03������Һ�У����������ͬ
D��25 ��ʱ��Ũ��Ϊ0.2mol/L��Na2CO3��Һ��ֻ����ˮ��ƽ�⣬�����ڵ���ƽ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com