

| A | B | C | D | |
| 物质 | 煤油 | 丙醇 | 四氯化碳 | 乙醚 |
| 沸点/℃ | 180~310℃ | 97.4 | 76.5 | 34.5 |
分析 (1)A.青蒿素和双氢青蒿素的分子式不同;
B.青蒿素与氢气发生加成反应生成双氢青蒿素;
C.根据结构简式确定分子式;
D.由结构简式可确定含有的环的数目.
(2)根据信息:水煎青蒿药性不稳定,效果差,改用乙醇控温60℃,药效显著提高来回答;
(3)根据:用乙醇煎青蒿控温60℃,药效显著结合物质的沸点知识来回答;
(4)根据物质分离的方法以及特点来回答.
解答 解:A.由结构简式可知青蒿素的分子式为C15H22O5,故A正确;
B.青蒿素与氢气发生加成反应生成双氢青蒿素,属于还原反应,故B正确;
C.由结构简式可知青蒿素分子中含有过氧链和酯基、醚键,故C正确;
D.由结构可知,青蒿素和双氢青蒿素含有3个六元环,故D错误;
故选D;
(2)水煎青蒿药性不稳定,效果差,改用乙醇控温60℃,药效显著,说明青蒿素具有可溶于乙醇、对热不稳定的性质,故答案为:可溶于乙醇、对热不稳定;
(3)乙醚的沸点低,当乙醚沸腾后,继续加热,乙醚的温度不会升高,避免由于温度高而破坏青蒿素的有效成分,故选D;
(4)用水、乙醇等从植物青蒿中提取青蒿素的方法是采用的物质在不同试剂中溶解度的大小差异来分离的,属于固-液萃取法 (或萃取法).
故答案为:固-液萃取法 (或萃取法).
点评 本题考查学生有机物的性质和结构、有机物的分离等知识,属于综合知识的考查,难度中等.


科目:高中化学 来源: 题型:解答题
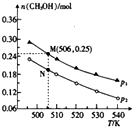 以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法.
以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑦⑨ | B. | ②④⑧⑩ | C. | ①③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
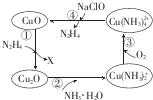 肼(N2H4)的性质类似于氨气,易溶于水,是塑料、橡胶发泡剂的原料.将肼蒸气通入Cu0胶体中,可发生如图所示的转化.
肼(N2H4)的性质类似于氨气,易溶于水,是塑料、橡胶发泡剂的原料.将肼蒸气通入Cu0胶体中,可发生如图所示的转化.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
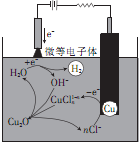 氧化亚铜(Cu2O)作为一种重要的无机化工原料,在徐料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:
氧化亚铜(Cu2O)作为一种重要的无机化工原料,在徐料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.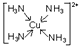 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com