
【题目】用生产钛白的副产品FeSO4与软锰矿(主要成分是MnO2)可制备高纯MnO2
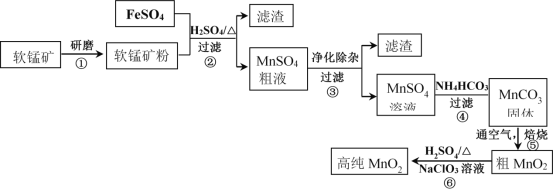
(1)步骤①中研磨的目的是______________________。
(2)步骤②中主要发生的反应是FeSO4与MnO2转化为MnSO4与__________。
(3)步骤②中Mn2+浸出率受初始H2SO4浓度与温度的影响如下图所示。
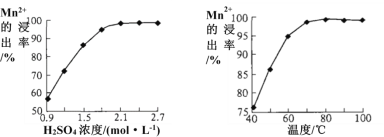
软锰矿粉酸浸的适宜条件是________________。
(4)步骤②中,若硫酸初始浓度小于1.8mol/L,反应进行一段时间后,有红褐色固体析出,其原因是____________。
(5)已知MnSO4粗液中还含有Al3+、Fe3+和Ni2+离子,溶液中离子生成氢氧化物的pH如下表:
Al(OH)3 | Fe(OH)3 | Ni(OH)2 | Mn(OH)2 | |
开始沉淀时pH | 3.4 | 1.5 | 6.9 | 8.2 |
完全沉淀时pH | 4.7 | 2.8 | 8.9 | 10.2 |
注:金属离子的起始浓度为0.1mol·L-1
步骤③进行的操作是:调节pH=5.4,过滤,滤渣中含_____________________。
(6)已知:几种难溶物的溶解平衡常数K
化学式 | MnCO3 | NiCO3 | MnS | NiS |
K | 2.24×10-11 | 1.42×10-7 | 4.65×10-14 | 1.07×10-21 |
步骤③还需加入的除杂试剂是_______固体(填序号)。
A.Na2CO3 B.MnCO3 C.Na2S D.MnS
(7)步骤⑤中焙烧MnCO3制MnO2,发生反应的化学方程式是_____________。
【答案】增大反应面积,加快化学反应速率 Fe2(SO4)3 硫酸浓度2.1mol/L,T=70℃ 随着反应进行,pH变大,Fe3+水解生成Fe(OH)3 Al(OH)3、Fe(OH)3 D 2MnCO3+O2![]() 2MnO2+2CO2
2MnO2+2CO2
【解析】
软锰矿粉碎后,能增大与硫酸亚铁、硫酸的接触面积,提高反应速率;软锰矿与硫酸亚铁反应生成硫酸锰和硫酸铁;通过调节pH,除去溶液中的铁离子,得到硫酸锰,在经过提纯得到高纯二氧化锰。
(1)步骤①中研磨使软锰矿变为细小颗粒,可增大反应面积,提高反应速率;
(2)步骤②中Mn的化合价降低,则Fe的化合价升高,则生成硫酸铁;
(3)根据图像信息,Mn2+浸出率高时,硫酸的浓度为2.1mol/L,温度为70℃;
(4)随反应的进行,硫酸越来越少,溶液的pH逐渐增大,铁离子水解程度增大,生成氢氧化铁的量增大;
(5)根据表中数据,调节pH=5.4,溶液中的Al3+、Fe3+完全变为沉淀,则滤渣的成分为Al(OH)3、Fe(OH)3;
(6)根据表中给定的Ksp,Ksp(MnS)>Ksp(NiS),加入MnS即可除去溶液中的Ni2+,答案为D;
(7)步骤⑤中通入空气焙烧MnCO3制MnO2,Mn的化合价升高,则空气中的氧气参与反应,化合价降低,反应的方程式为2MnCO3+O2![]() 2MnO2+2CO2。
2MnO2+2CO2。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示。
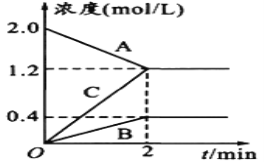
由图中数据
(1)该反应的反应物是___________。
(2)该反应是否可逆反应_____(填“是”或“否”),原因是__________________。写出该反应的化学方程式________________________。
(3)反应开始至2min,用C表示化学平均反应速率为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是重要的工业原料,在实验室里探究在高温下绿矾的分解产物。
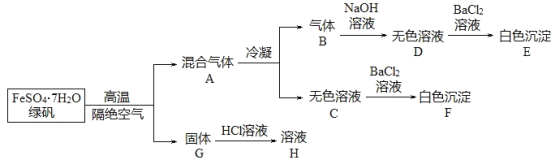
取27.8g绿矾晶体,按上述流程进行实验,测得白色沉淀E和F的质量分别为10.85g和11.65g。
(1)通过计算,写出绿矾隔绝空气高温分解的反应方程式:______。
(2)实验室检验溶液H中金属阳离子的步骤和现象:______。
(3)白色沉淀E在空气中放置一段时间后称量,发现质量大于10.85g,用化学方程式来解释这个现象:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒容密闭容器中发生反应:2NO2(g)![]() 2NO(g)+O2(g)(NO2红棕色气体,NO无色气体),下列状态中不能表明该反应达到平衡状态的有( )
2NO(g)+O2(g)(NO2红棕色气体,NO无色气体),下列状态中不能表明该反应达到平衡状态的有( )
A.混合气体的颜色不再改变的状态
B.单位时间内生成nmolO2的同时生成2nmolNO2
C.混合气体的密度不再改变的状态
D.混合气体的平均相对分子质量不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是
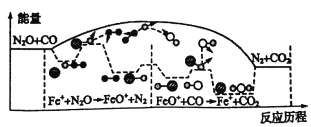
A. 反应总过程△H<0
B. Fe+使反应的活化能减小
C. 总反应若在2L的密闭容器中进行,温度越高反应速率一定越快
D. Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为放热及应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应的叙述正确的是( )
A.SO2与Ba(NO3)2反应生成BaSO3
B.NH3在纯O2中燃烧生成NO2
C.过量CO2与氨水反应生成NH4HCO3
D.高温条件下Fe与水蒸气反应生成Fe(OH)3和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 向苯酚钠溶液中滴加NaHSO3溶液,溶液变浑浊 | 苯酚酸性弱于H2SO3酸性 |
B | 向AgNO3溶液中逐滴加入浓度均为0.05 mol·L-1的NaI、NaCl混合溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
C | 向FeCl3溶液中加入Cu粉,Cu粉溶解 | Cu的还原性大于Fe |
D | 向盛有H2O2溶液的试管中滴几滴酸化的FeCl2溶液,溶液变成棕黄色,一段时间后,溶液中有气泡出现 | 铁离子催化H2O2的分解 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种含酰亚胺结构的对苯二胺衍生物的合成路线,其产物(F)可作为一种空腔孔径较大的新型大环芳酰胺的合成原料。
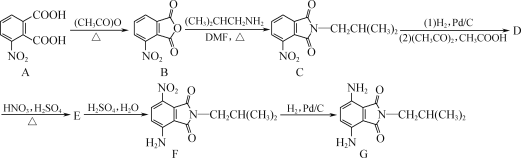
(1)A中官能团的名称为________和________。
(2)F→G的反应类型为________。
(3)D的分子式为C14H16N2O3,写出D的结构简式:________。
(4)A的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:________。
①能与FeCl3溶液发生显色反应;
②含有苯环,且苯环上含有硝基;
③含有三种不同化学环境的氢原子。
(5)写出以甲苯、邻二甲苯,制备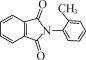 (无机试剂和DMF,(CH3CO)2O及有机溶剂任用,合成路线流程图示例见本题题干)________。
(无机试剂和DMF,(CH3CO)2O及有机溶剂任用,合成路线流程图示例见本题题干)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Fe3+/Fe2+作为氧化还原介质,可以在低电位条件下电解HCl制取Cl2,其原理如图所示,下列说法正确的是( )
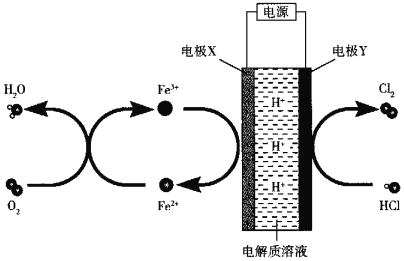
A.X极上的电势比Y极上的低
B.![]() 向Y极迁移,X极周围溶液pH升髙
向Y极迁移,X极周围溶液pH升髙
C.X极上发生反应:![]()
D.电解总反应为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com