
【题目】如下图所示,在试管甲中先加入2 mL 95%的乙醇,在摇动的情况下缓缓加入5 mL浓硫酸,并充分摇匀。冷却后再加入2 g无水CH3COOH,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入7 mL饱和碳酸钠溶液。按图连接好装置。

用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验。
(1)甲试管主要化学反应方程式__________________________。
(2)加入浓硫酸的目的是________、_________。
(3)试管乙中观察到的现象是____________________________。
(4)导气管要在饱和碳酸钠溶液的液面上,不能插入溶液中,其目的是____________。
(5)饱和碳酸钠溶液的作用是(填字母)________。
A.中和浓硫酸
B.中和乙酸并吸收乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
【答案】 CH3COOH+C2H5OH CH3COOC2H5+H2O 催化剂 吸水剂 液体分层,上层为无色透明的油状液体 防止倒吸 BC
CH3COOC2H5+H2O 催化剂 吸水剂 液体分层,上层为无色透明的油状液体 防止倒吸 BC
【解析】该实验的目的是制备乙酸乙酯。
(1)甲试管中,乙酸和乙醇反应,主要化学反应方程式为:CH3COOH+C2H5OH CH3COOC2H5+H2O ;
CH3COOC2H5+H2O ;
(2)此反应是可逆反应,为使平衡向右移动,将生成的水移走,增大产率,故加入浓硫酸的目的是作催化剂和吸水剂;
(3)甲中生成的乙酸乙酯蒸汽到了试管乙中冷凝,因其难溶于水且密度小于水,故现象是液体分层,上层为无色透明的油状液体;
(4)导气管要在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止倒吸;
(5)甲中除了产物到了乙试管中,乙醇、乙酸也会被蒸出来到乙中,乙醇易溶于水,而乙酸可以和碳酸钠反应生成乙酸钠溶液,故饱和碳酸钠溶液的作用是:中和乙酸并吸收乙醇、乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出,故选BC。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】中学化学中有很多物质可以实现下图中物质之间的转化。其中反应条件和部分反应的产物已略去。液体B和C可能是单一溶质的溶液,也可能是纯净物。

(1)若A是一种红色金属,气体D能使品红溶液褪色,加热时又恢复原色。写出反应①的化学方程式_______________________________________________。
(2)若A是金属单质,D是一种无色气体,遇到空气变为红棕色,液体C呈浅绿色。
写出反应①的离子方程式________________________________________; 写出反应②的任意一个离子方程式____________________________________________。
(3)若A是一种金属单质,D是最轻的气体,B能否是NaOH溶液________(填“能”或“否”),若能,写出相应的离子方程式 (若否,则不用填此空)__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M,N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )

A. 反应的化学方程式为:2MN B. t2时,正逆反应速率相等,达到平衡
C. t3时,正反应速率大于逆反应速率 D. t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W,X,Y,Z的原子序数依次增大,W,X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是( )
A.简单离子半径:W<X<Z
B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:W<Y
D.最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A.浓溶液一定是饱和溶液
B.析出晶体的溶液是饱和溶液
C.任何物质的饱和溶液,加热后都变成不饱和溶液
D.饱和溶液中,溶质的溶解速率大于结晶速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图.已知烃B在标准状况下的密度为1.16gL﹣1 , C能发生银镜反应,F为有浓郁香味,不易溶于水的油状液体. 
请回答:
(1)有机物D中含有的官能团名称是 .
(2)D+E→F的反应类型是 .
(3)有机物A在高温下转化为B的化学方程式是 .
(4)下列说法正确的是 .
A.有机物E与金属钠反应比水与金属钠反应要剧烈
B.有机物D、E、F可用饱和Na2CO3溶液鉴别
C.实验室制备F时,浓硫酸主要起氧化作用
D.有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】参考如图,按要求回答下列问题: 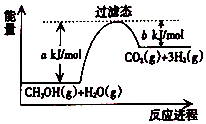
(1)甲醇质子交换膜燃料电池将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O反应生成CO2和H2 . 若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是(填“增大”、“减小”、“不变”),反应热△H的变化是(填“增大”、“减小”、“不变”).请写出CH3OH(g)和H2O(g)反应的热化学方程式 .
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的另一种反应原理是:
CH3OH(g)+ ![]() O2(g)CO2(g)+2H2(g)△H=﹣c kJ/mol
O2(g)CO2(g)+2H2(g)△H=﹣c kJ/mol
又知H2O(g)H2O(l)△H=﹣d kJ/mol.
则甲醇燃烧热的热化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com