
分析 (1)反应中生成的气体都是氢气,根据n=$\frac{V}{{V}_{m}}$分别计算出生成氢气的物质的量,然后利用电子守恒可计算出转移电子的物质的量;
(2)Mg与氢氧化钠溶液反应,则6.72L气体为铝与氢氧化钠溶液反应生成的,而Al与盐酸、氢氧化钠溶液反应生成的氢气体积相等,据此可计算出Mg与盐酸反应生成氢气的体积,然后根据反应方程式分别进行计算即可.
解答 解:(1)反应中生成的气体都是氢气,当混合物与盐酸反应时生成氢气的物质的量为:$\frac{8.96L}{22.4L/mol}$=0.4mol,根据电子守恒可知反应转移电子的物质的量为:0.4mol×2=0.8mol;
与NaOH溶液反应生成标准状况下6.72L氢气,氢气的物质的量为:时转移电子总物质的量为:$\frac{6.72L}{22.4L/mol}$=0.3mol,根据电子守恒,转移电子的物质的量为:0.3mol×2=0.6mol,
故答案为:0.80;0.60;
(2)Al、Mg都与盐酸反应产生氢气,但只有Al与氢氧化钠溶液反应产生氢气,又由于等质量铝与盐酸、氢氧化钠反应产生的氢气体积相同,都为6.72 L,则镁产生的氢气为:8.96 L-6.72 L=2.24 L,
设Mg的质量为x,Al的质量为y,
Mg+2HCl=MgCl2+H2↑
24g 22.4L
x 2.24 L
则:x=2.4 g,
2Al+6HCl═2AlCl3+3H2↑ 或2Al+2NaOH+2H2O═2NaAlO2+3H2
54g 67.2 L 54g 67.2 L
y 6.72 L y 6.72 L
则y=5.4g,
答:混合物中Mg的质量为2.4g,铝的质量为5.4g.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的化学计算能力.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
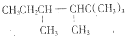 f.C8H10O2
f.C8H10O2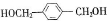 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、I-、NO3-、SiO32- | B. | Ag+、Fe3+、Cl-、SO42- | ||
| C. | K+、SO42-、Cu2+、NO3- | D. | NH4+、OH-、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醛、乙酸 | B. | 乙醇、乙二醇 | C. | 甲烷、丙炔 | D. | 苯、乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
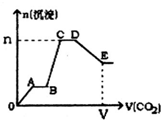
| A. | A~B段和C~D段发生的反应相同 | |
| B. | B~C段反应的离子方程式是 A1O2-+2H2O+CO2═Al(OH)3↓+HCO3- | |
| C. | V=134.4L,n=3mol | |
| D. | D点所得溶液中离子浓度关系为c(K+)>c(CO${\;}_{3}^{2-}$)>c(OH-)>c(HCO${\;}_{3}^{-}$)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
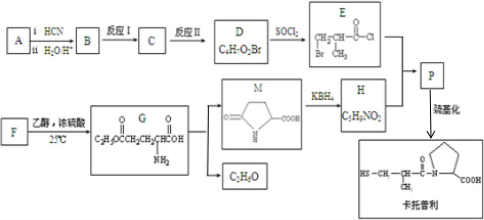
 (R1、R2为烃基)
(R1、R2为烃基)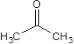 .
. ,反应Ⅱ所用试剂是HBr.
,反应Ⅱ所用试剂是HBr. .
.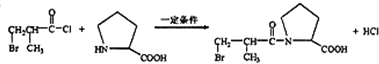 .
. (任写一种).
(任写一种).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com