
(10分)硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为: H2SO4=H++HSO4-,HSO4- H++SO42-。.
H++SO42-。.
请据此回答下列有关问题:
(1)Na2SO4溶液呈 (填“弱酸性”、“中性”或“弱碱性”),原因是: (用离子方程式表示)。
(2)写出H2SO4溶液与BaCl2溶液反应的离子方程式: ;
(3)在0.1 mol·L-1的Na2SO4溶液中,下列粒子浓度关系式正确的是 。(填编号)
A.c(SO42-)+c(HSO4-)=0.1 mol·L-1
B.c(SO42-)+c(HSO4-)=2c(Na+)
C.c(OH-)=c(H+)+c(HSO4-)
D.c(Na+)+c(H+)=c(OH-)+c(HSO4-)
(4)已知0.1 mol·L-1的NaHSO4溶液的pH=2,则0.1 mol·L-1的H2SO4溶液中SO42-的浓度 0.01mol·L-1(填“>”“=”或“<”),原因是 。
(10分 (1) 弱碱性 ,SO42- + H2O  HSO4—+ OH—
HSO4—+ OH—
(2)HSO4- + Ba2+ = BaSO4↓+ H+ (3)AC
(4)<(1分),硫酸第一步电离的H+对第二步的电离产生抑制作用
【解析】
试题分析:(1)根据硫酸的第一步电离是完全的:H2SO4=H++HSO4-,第二步电离并不完全:HSO4-?H++SO42-,则
Na2SO4溶液存在SO42-+H2O?OH-+HSO4-,溶液呈弱碱性,答案为:弱碱性;SO42-+H2O?OH-+HSO4-;
(2)硫酸中存在HSO4-离子,难电离,硫酸与氯化钡溶液反应的离子方程式为:HSO4-+Ba2+=BaSO4↓+H+,答案为:HSO4-+Ba2+=BaSO4↓+H+;
(3)A.依据物理守恒,c(SO42-)+c(HSO4-)=0.1 mol·L-1 ,A正确;B、依据物料守恒,c( Na+)=2c(SO42-)+2c(HSO4-),B错误;C.依据质子守恒c(OH-)=c(H+)+c(HSO4-),C正确; D、溶液中存在电荷守恒:c( Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-),D错误;选AC。
(4)因为0.1 mol·L-1的NaHSO4溶液的pH=2,根据HSO4-?H++SO42-,电离出的硫酸根离子的浓度为0.01 mol·L-1,0.1 mol·L-1的H2SO4溶液中
H2SO4 = H++ HSO4-,第二步不完全电离 HSO4-? H++ SO42-
0.1 0.1 0.1 0.1 0.01
所以SO42-的浓度 < 0.01mol·L-1,原因是硫酸第一步电离的H+对第二步的电离产生抑制作用。
考点:考查弱电解质的电离,离子反应方程式,溶液中粒子浓度的关系。


科目:高中化学 来源:2014-2015学年宁夏回族自治区银川一中高一上期中化学试卷(解析版) 题型:选择题
某无色透明酸性溶液中,能大量共存的离子组是
A.Na+、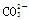 、Cu2+、
、Cu2+、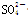 B.K+、Fe3+、
B.K+、Fe3+、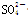 、OH-
、OH-
C.Ca2+、NO3-、Cl-、K+ D.Ba2+、K+、MnO4_、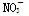
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏回族自治区银川一中高二上学期期中化学试卷(解析版) 题型:选择题
在气体反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是
①增大反应物的浓度 ②升高温度 ③增大压强 ④移去生成物 ⑤加入正催化剂
A.①②③ B.②③⑤ C.②⑤ D.②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏高邮市高一上学期期中调研测试化学试卷(解析版) 题型:选择题
下列各组离子在溶液中能大量共存的是
A.H+、Na+、HCO3-、Cl- B.Cu2+、Na+、Cl-、SO42-
C.Mg2+、K+、SO42-、OH- D.Ag+、Al3+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏高邮市高一上学期期中调研测试化学试卷(解析版) 题型:选择题
在日常生活中会接触到许多物质。下列物质中属于酸性氧化物的是
A.硫酸铵 B.水 C.二氧化碳 D.氧化铜
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中化学试卷(解析版) 题型:选择题
SO2通过下列工艺流程可以制取化工原料H2SO4和清洁能源H2。下列说法正确的是
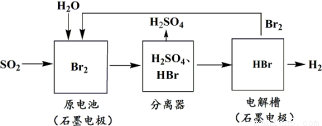
A.电解槽中也可以用铁电极代替石墨作为阳极
B.原电池中负极的电极反应为:SO2+2H2O-4e-=SO42-+4H+
C.该工艺流程用总反应的化学方程式表示为:SO2+Br2+2H2O=2HBr+H2SO4
D.该生产工艺的优点是Br2被循环利用,原电池产生的电能可以充分利用,还能获得清洁能源
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中化学试卷(解析版) 题型:选择题
将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量的变化趋势,错误的是

查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高一上学期月考化学试卷(解析版) 题型:填空题
选择下列实验方法分离物质,将分离方法的序号填在横线上
A 萃取分液法 B 结晶法 C 分液法 D 蒸馏法 E 过滤法
①_____分离饱和食盐水与沙子的混合物。
②_____分离水和汽油的混合物。
③_____分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
④____从碘的水溶液里提取碘。
⑤_____从硝酸钾和氯化钠的混合液中获得硝酸钾。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省中山市高二上学期月考化学试卷(解析版) 题型:选择题
下列事实能说明碳酸的酸性比乙酸弱的是:
A.乙酸能发生酯化反应,而碳酸不能
B.碳酸和乙酸都能与碱反应
C.乙酸易挥发,而碳酸不稳定易分解
D.乙酸和Na2CO3反应可放出CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com