
【题目】在某澄清透明的酸性溶液中,能共存的离子组是
A.NH4+、Cl-、Fe3+、K+ B.Na+、SO32-、K+、Cl-
C.MnO4-、Fe2+、Na+、SO42- D.K+、SO42-、HCO3-、Na+
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是

A. ①是其它条件一定时,反应速率随温度变化的图象,正反应△H<0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C. ③是在有无催化剂存在下建立的平衡过程图象,曲线a是使用催化剂的曲线
D. ④是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1>p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为2 L的密闭容器中充入2 mol SO2和1 mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g)![]() 2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
A. 充入2 mol SO3后,SO2的物质的量增大
B. 第一次反应达到平衡时共放出热量176.4 kJ
C. 充入2 mol SO3达到新平衡时,容器内的压强为1.4p
D. 降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸生产中,500℃时,NH3和O2可能发生如下反应:
① 4NH3 (g) + 5O2 (g) ![]() 4NO (g) + 6H2O (g) △H= - 9072 kJ·mol-1K= 1.1×1026
4NO (g) + 6H2O (g) △H= - 9072 kJ·mol-1K= 1.1×1026
② 4NH3 (g) + 4O2 (g) ![]() 2N2O (g) + 6H2O (g) △H= - 1105 kJ·mol-1K= 4.4×1028
2N2O (g) + 6H2O (g) △H= - 1105 kJ·mol-1K= 4.4×1028
③ 4NH3 (g) + 3O2 (g) ![]() 2N2 (g) + 6H2O (g) △H= - 1269 kJ·mol-1K= 7.1×1034
2N2 (g) + 6H2O (g) △H= - 1269 kJ·mol-1K= 7.1×1034
其中,②、③是副反应。若要减少副反应,提高NO的产率,最合理的措施是
A.减小压强 B.降低温度
C.增大O2浓度 D.使用合适的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里保存下列试剂,其保存的方法和理由,描述都正确的是
编号 | 试剂 | 保存方法 | 理由 |
A | 水玻璃 | 存放在带橡皮塞的细口瓶中,密封 | 防止与空气接触被氧化和与二氧化碳接触而变质 |
B | 硫酸亚铁晶体 | 存放在带玻璃塞的广口瓶中,密封 | 防止与空气接触被氧化 |
C | 浓硫酸 | 密闭保存 | 防止吸水和挥发 |
D | 新制的溴水 | 存放在无色试剂瓶中,密封 | 防止挥发 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学反应A2(g)+2B2(g)=2AB2(g) (A2、B2、AB2的结构式分别为A=A、B-B、B-A-B),能量变化如图所示,下列有关叙述中正确的是
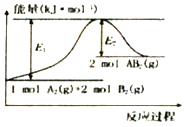
A. 该反应若生成2molAB2(g)则吸收的热量为(El-E2)kJ
B. 该反应的进行一定需要加热或点燃条件
C. 该反应断开化学键消耗的总能量小于形成化学键释放的总能量
D. 生成2molB-B键放出E2kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为CH2=CH— CH2OH。下列关于该有机物的叙述不正确的是
A.能与金属钠发生反应并放出氢气
B.能在催化剂作用下与H2发生加成反应
C.在浓H2SO4催化下能与乙酸发生酯化反应
D.能发生银境反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,向容积为2L的密闭容器中充入一定量的X气体和Y气体,发生如下反应:
X(g)+2Y(g)![]() Z(g)
Z(g)
反应过程中测定的部分数据见下表:
反应时间/min | n(X)/mol | n(Y)/ mol |
0 | 2.00 | 2.40 |
10 | 1.00 | |
30 | 0.40 |
下列说法正确的是
A.前10 min内反应的平均速率为v(Z)=0.10 mol·L-1·min-1
B.温度为200℃时,上述反应平衡常数为20,则正反应为吸热反应
C.若密闭容器体积可变,其他条件不变,在达到平衡后缩小容器体积为原来一半,则c(X)<1mol/L
D.保持其他条件不变,向容器中再充入1.00 mol X气体和1.20 mol Y气体,到达平衡后,X转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com