
【题目】下列氢键从强到弱的顺序正确的是
①O—H…O ②N—H…N ③F—H…F ④O—H…N
A. ①②③④B. ③①④②C. ③②④①D. ③④①②
科目:高中化学 来源: 题型:
【题目】将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)右图是某同学画出CO分子中氧原子的核外电子排布图,
![]()
请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
(2)写出两种与CO互为等电子体的离子 。
(3)向CuSO4溶液中加入足量氨水可得到深蓝色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > > (填元素符号)。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是 ;在甲醇分子中碳原子轨道的杂化类型为 。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:
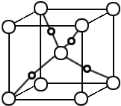
①在该晶胞中,Cu+ 的配位数是 ,
②若该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下面的实验过程完成下题:

(1)写出上述过程颜色变化(a)________;(b)______;(d)________。
(2)写出上述反应的化学方程式:(1)____________;(3)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验,并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:
物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
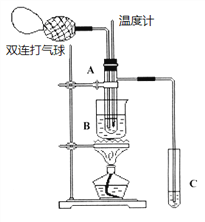
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)____________________________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A中的位置,在实验开始时,为控制并测量反应溶液的温度,温度计水银球的位置应在_____________;当试管A中的主要反应完成后,为在C中收集乙酸,温度计水银球的位置应在______________,该操作名称为 _____________;烧杯B内盛装的液体可以是____________(写出一种即可,在题给物质中找);
(3)乙酸是非常重要的工业原料,其氯代物——氯乙酸可在工业上生产食品香精菠萝酯(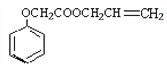 ),实验室模拟工业简易流程如下:
),实验室模拟工业简易流程如下:
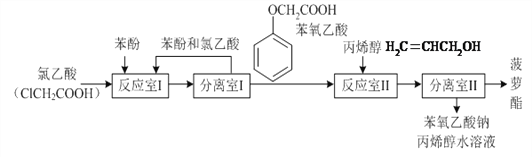
反应室I中发生反应的反应类型是___________。
分离室II的操作为:①用NaHCO3溶液洗涤后分液;②有机层用水洗涤后分液;
洗涤时不能用NaOH溶液代替NaHCO3溶液,其原因是__________________________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下物质分类组合正确的是 ( )
A | B | C | D | |
强电解质 | HCl | FeCl3 | H3PO4 | HClO |
弱电解质 | HF | CH3COOH | NH3·H2O | Ba(OH)2 |
非电解质 | C2H5OH | Zn | H2O | SO3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 31g白磷(![]() )分子中含有1 NA 个P-P键
)分子中含有1 NA 个P-P键
B. 1molFeI2与1molCl2反应时转移的电子数为3NA
C. 标准状况下,4.48LCH4和乙烯(CH2=CH2)的混合气体完全燃烧,产生的水中所含O-H键数目为0.8NA
D. 常温下,将1 mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属硫化物和硫酸盐在工农业生产中有广泛应用。
(1)二硫化钼(MoS2)是重要的固体润滑剂。
向体积为2L的恒容密闭容器中加入0.1molMoS2、0.2molNa2CO3,并充入0.4molH2,
发生反应:MoS2(s)+2Na2CO3(s)+4H2(g)![]() Mo(s) +2CO(g) + 4H2O(g) + 2Na2S(s) △H =akJ mol-1,测得在不同温度下达到平衡时各气体的物质的量分数如图所示。
Mo(s) +2CO(g) + 4H2O(g) + 2Na2S(s) △H =akJ mol-1,测得在不同温度下达到平衡时各气体的物质的量分数如图所示。
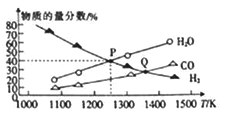
①a________0(填“<”“>”“=”,下同)。
②容器内的总压:P点________Q点。
③P点对应温度下,H2的平衡转化率为________,平衡常数K=________。
(2)辉铜矿(主要成分是Cu2S)在冶炼过程中会产生大量的SO2。已知冶炼过程中部分反应为:
①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) △H=-768.2kJ/mol
②2Cu2O+Cu2S(s)=6Cu(s)+SO2(g) △H=+116kJ/mol,则Cu2S与O2反应生成Cu与SO2的热化学方程式为___________________________。
(3)回收处理SO2的方法之一是用氨水将其转化为NH4HSO3。已知常温下 Kb(NH3H2O) =1.5×l0-5 Ka1(H2SO3) =1.6×l0-2 Ka2(H2SO3)=1×10-7,若吸收过程中氨水与SO2恰好完全反应,则所得溶液在常温下的pH________7(填“>”“ <”或“=”,下同),溶液中c(SO32-)________c(H2SO3)。
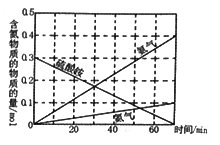
(4)在500℃下硫酸铵分解会得到4种产物,其含氮物质的物质的量随时间的变化如上图所示。则该条件下硫酸铵分解的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于盐类水解反应说法正确的是
A.任何盐都可发生水解反应
B.盐只能发生水解反应而不能发生其他反应
C.盐水解反应肯定能破坏水的电离平衡且促进水的电离
D.盐的水溶液为中性时,则盐一定不发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,最适合的氧化剂是
A.H2O2水溶液 B.KMnO4溶液
C.Cl2水溶液 D.HNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com