
下列叙述正确的是( )
A.Fe分别与氯气和稀盐酸反应得到不同的氯化物
B.某无色溶液中通入Cl2,溶液变为淡黄色,再加入淀粉溶液,溶液变为蓝色,说明原溶液中存在I-
C.CO2、NO2、SO2都能与H2O反应,其反应原理相同
D.C、N、S三种单质直接与O2反应都能生成两种氧化物
科目:高中化学 来源: 题型:
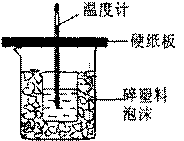
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是____________,烧杯间填满碎塑料泡沫的作用是_________________________。
(2) 大烧杯上如不盖硬纸板,则求得的中和热数值_______(填“偏大”、“偏小’、“无影响”)
(3) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上述实验相比,所求中和热的数值会________(填“相等”或“不相等”),理由是______________________。
(4)设50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液反应的反应热为△H1,25mL0.5mol/L的浓硫酸与50mL0.55mol/L的NaOH溶液反应的反应热为△H2, 50mL0.5mol/L的醋酸与50mL0.55mol/L的NaOH溶液反应的反应热为△H3,则△H1、△H2、△H3的关系是 。(用“>”“<”或“=”连接)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的现象或反应,与原理解释符合因果关系的是( )
| 现象或反应 | 原理解释 | |
| A | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝的金属性不活泼,不能与氧气反应[来源:学|科|网] |
| B | 硫与氧气只有在加热条件下才能进行反应 | 该反应为吸热反应 |
| C | 向碳酸钠和氢氧化钠溶液中滴加酚酞,溶液都呈红色 | 碳酸钠和氢氧化钠都是碱 |
| D | 常温下,铝制容器可用于盛装冷的浓硫酸 | 常温下,铝遇冷的浓硫酸发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验的现象与对应结论均不正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显现象 | Al与浓硝酸发生钝化 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中,满足下图物质一步转化关系的选项是( )
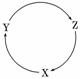
| 选项 | X | Y | Z |
| A | Na | NaOH | NaHCO3 |
| B | Cu | CuSO4 | Cu(OH)2 |
| C | C | CO | CO2 |
| D | Si | SiO2 | H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,设计了下图所示装置进行有关实验:
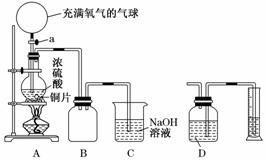
(1)先关闭活塞a,将6.4 g铜片和10 mL 18 mol/L的浓硫酸放在圆底烧瓶中共热至反应完成,发现烧瓶中还有铜片剩余。再打开活塞a,将气球中的氧气缓缓挤入圆底烧瓶,最后铜片完全消失。
①写出上述过程中圆底烧瓶内发生反应的化学方程式:
打开活塞a之前___________________________________________________;
打开活塞a之后___________________________________________________。
②B是用来收集实验中产生的气体的装置,但集气瓶内的导管未画全,请直接在图上把导管补充完整。
(2)实际上,在打开活塞a之前硫酸仍有剩余。为定量测定余酸的物质的量,甲、乙两学生进行了如下设计:
①甲学生设计的方案是:先测定铜与浓硫酸反应产生SO2的量,再通过计算确定余酸的物质的量。他测定SO2的方法是将装置A产生的气体缓缓通过装置D,从而测出装置A产生气体的体积(已折算成标准状况下)。你认为甲学生设计的实验方案中D装置中的试剂为______________________(填化学式)。
②乙学生设计的方案是:将反应后的溶液冷却后全部移入到烧杯中稀释,并按正确操作配制100 mL溶液,再取20 mL于锥形瓶中,用________作指示剂,用标准氢氧化钠溶液进行滴定[已知:Cu(OH)2开始沉淀的pH约为5],选择该指示剂的理由为__________________________________________________;再求出余酸的物质的量,若耗去a mol/L氢氧化钠溶液b mL,则原余酸的物质的量为________mol(用含a、b的表达式来表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下面的反应路线及所给信息填空。

(1)A的结构简式是________,名称是________。
(2)①的反应类型是________,②的反应类型是________。
(3)反应④的化学方程式是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
丙烯醇(CH2===CH—CH2OH)可发生的化学反应有
( )
①加成 ②氧化 ③燃烧 ④加聚 ⑤取代
A.仅①②③ B.仅①②③④
C.①②③④⑤ D.仅①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质能发生消去反应,但不能发生催化氧化反应的是
( )
A.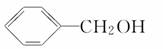
B.(CH3)2CHOH
C.CH3CH2C(CH3)2CH2OH
D.CH3CH2C(CH3)2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com