
科目:高中化学 来源: 题型:选择题
| A. | 合成氨工业中使用催化剂 | |
| B. | 用铁粉代替铁钉与稀硫酸反应制取氢气 | |
| C. | 食品放在冰箱中贮藏 | |
| D. | 进行铝和盐酸反应时,稍微加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +1,+3 | B. | +3,+1 | C. | +2,+3 | D. | +3,+2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
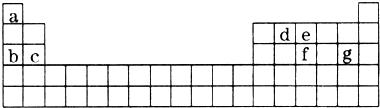
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16gCH4中含有4NA个C-H键 | |
| B. | 常温常压下,4g氦气所含有的质子数目为4 NA | |
| C. | 18gD2O所含的中子数为10NA | |
| D. | Fe-Cu和硫酸铜溶液构成的原电池中,若生成2g H2,则转移的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,7.8 g 固体Na2O2 中,含有的阴阳离子总数为0.4 NA | |
| B. | 4℃时,18 g 2H216O中含有共用电子对数为2 NA | |
| C. | 标准状况下6.72L HF的分子数为0.3 NA | |
| D. | 常温下,32 g O2与32 g O3所含的氧原子数都为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
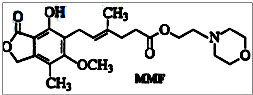
| A. | MMF属于有机高分子化合物 | |
| B. | MMF能发生取代反应和加成反应 | |
| C. | 1molMMF能与6mol氢气发生加成反应 | |
| D. | 1molMMF能与含3molNaOH的水溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 在上述条件下,SO2不可能100%地转化为SO3 | |
| C. | 化工生产中,可通过改变温度、浓度、压强等因素,提高SO2的转化率 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com