
| A. | SO2 | B. | CH4 | C. | NH3 | D. | SO42- |
分析 中心原子的杂化类型为sp3,说明该分子中心原子的价层电子对个数是4,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.
解答 解:A.SO2中S原子价层电子对个数=2+$\frac{1}{2}$(6-2×3)=3,所以S原子采用sp2杂化,故A选;
B.CH4分子中C原子价层电子对个数=4+$\frac{1}{2}$(4-4×1)=4,所以C原子采用sp3杂化,故B不选;
C.氨气分子中氮原子价层电子对个数=3+$\frac{1}{2}$(5-3×1)=4,所以N原子采用sp3杂化,故C不选;
D.硫酸根离子中硫原子价层电子对个数═4+$\frac{1}{2}$(6+2-4×2)=4,所以S原子采取sp3杂化,故D不选;
故选A.
点评 本题考查了分子或离子中原子轨道杂化类型的判断,根据价层电子对互斥理论来分析,注意选项是D硫酸根离子中硫原子价层电子对个数的计算,为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CH≡CH+H2O $→_{△}^{HgSO_{4}}$CH3CHO | |
| B. | C2H5Br+H2O $→_{△}^{NaOH}$ C2H5OH+HBr | |
| C. | CaC2+2H2O→Ca(OH)2+C2H2↑ | |
| D. | CH3COOCH3+H2O$→_{△}^{催化剂}$CH3COOH+CH3OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
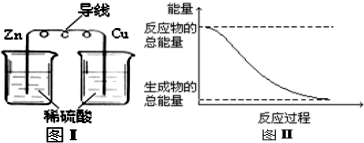
| A. | 化学反应中能量变化的主要原因是化学键的断裂与生成 | |
| B. | 化石燃料是可再生性能源,燃烧时将化学能转变为热能 | |
| C. | 图I所示的装置不能将化学能转变为电能 | |
| D. | 图II所示的反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠可能最多 | B. | 铝铁不可能一样多 | ||
| C. | 铝一定最多 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该装置电流表中没有电流通过 | |
| B. | 铝箔是正极 | |
| C. | 总反应为4Al+3O2+6H2O═4Al(OH)3 | |
| D. | 电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火 | |
| B. | 纳米铁粉可以高效地去除被污染水体的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附 | |
| C. | 为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用滴管滴加蒸馏水至刻度线 | |
| D. | Ba2+浓度较高时危害健康,但BaSO4可服入体内,做为造影剂用于X-射线检查肠胃道疾病 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g D2O所含的电子数为10NA | |
| B. | 12 g金刚石中含C-C键数为4NA | |
| C. | 标况下11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯的混合气体共14 g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀H2SO4反应 | B. | 灼热的炭与CO2反应 | ||
| C. | 高温煅烧石灰石 | D. | 甲烷在O2中的燃烧反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com