
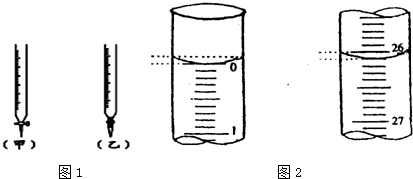
| 锥形瓶中溶液 | 滴定管中溶液 | 指示剂 | 滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 石蕊 | (乙) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
| A、常温常压下,48 g O3含有的氧原子数约为3NA |
| B、常温常压下,11.2 L乙烯(C2H4)含有2NA个碳原子 |
| C、1.7 g氨气所含有的电子数目为10 NA |
| D、2.7g铝与足量氢氧化钠溶液反应转移的电子数NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
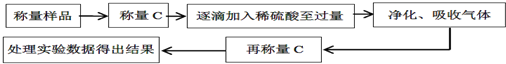
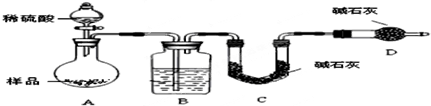
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知2H2(g+O2(g)=2H2O(g)△H=-483.6kJ/mol,则H2的燃烧热为241.8kJ/mol |
| B、稀氢氧化钠溶液与稀盐酸溶液中和,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol |
| C、应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D、需要加热才能发生的反应不一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、量筒 | B、容量瓶 |
| C、滴定管 | D、以上均不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.784 | B、0.896 |
| C、1.00 | D、1.12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com