

 )是合成APM的原料之一.APM的结构简式如图1所示.
)是合成APM的原料之一.APM的结构简式如图1所示.
 ,所以该有机物与氨基乙酸1:1反应形成六元环为:
,所以该有机物与氨基乙酸1:1反应形成六元环为: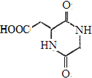 ;
; 和信息中的氰化物的反应可知,E的结构简式为
和信息中的氰化物的反应可知,E的结构简式为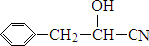 ,E由D与HCN加成而得,可推知D的结构简式为
,E由D与HCN加成而得,可推知D的结构简式为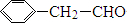 ;D由C催化氧化而得,则C为
;D由C催化氧化而得,则C为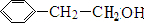 ;B水解得到C,则B为
;B水解得到C,则B为 ,所以A为
,所以A为 ;③中某苯的同系物苯环上的一硝基取代物只有一种,该硝基取代物W是苯丙氨酸的同分异构体,由此可知苯的同系物的侧链上共有3个C原子,苯的同系物有多种结构,但苯环上含有一种氢原子,应该满足对称结构,所以该苯同系物是1,3,5-三甲苯,据此进行解答.
;③中某苯的同系物苯环上的一硝基取代物只有一种,该硝基取代物W是苯丙氨酸的同分异构体,由此可知苯的同系物的侧链上共有3个C原子,苯的同系物有多种结构,但苯环上含有一种氢原子,应该满足对称结构,所以该苯同系物是1,3,5-三甲苯,据此进行解答.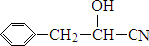 ,E由D与HCN加成而得,可推知D的结构简式为
,E由D与HCN加成而得,可推知D的结构简式为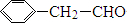 ;D由C催化氧化而得,则C为
;D由C催化氧化而得,则C为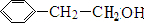 ;B水解得到C,则B为
;B水解得到C,则B为 ,所以A为
,所以A为 ,
, ,因此该有机物与氨基乙酸1:1反应形成六元环时,形成的环状化合物为:
,因此该有机物与氨基乙酸1:1反应形成六元环时,形成的环状化合物为: ,
, ;
; ;D为
;D为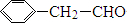 ,1molD物质完全燃烧消耗的氧气为9.5mol,
,1molD物质完全燃烧消耗的氧气为9.5mol, ;9.5;
;9.5; ,
, ;
; ,
, .
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 )的合成路线如下:
)的合成路线如下: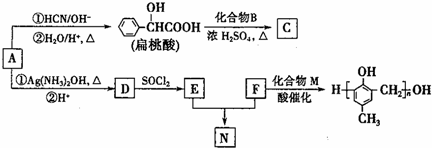
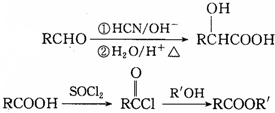 (R、R’代表烃基)
(R、R’代表烃基)查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液体积/mL | 盐酸标准溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+一定存在 |
| B、100mL溶液中含0.01mol CO32- |
| C、Cl-一定存在 |
| D、Fe3+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al→Al2O3→Al(OH)3→NaAlO2 |
| B、Cu→CuO→Cu(OH)2→CuSO4 |
| C、Na→Na2O2→NaOH→Mg(OH)2 |
| D、Fe→Fe2O3→Fe(OH)3→FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化铝陶瓷、氮化硅陶瓷都属于新型无机非金属材料 |
| B、煤矿井下的瓦斯爆炸主要是氢气燃烧引起的 |
| C、成熟的苹果能够释放出具有催熟作用的乙烯气体 |
| D、在粉尘较多的工作场所,工作人员易患硅肺病 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2通入FeSO4溶液中 |
| B、CO2通入Ca(OH)2溶液中 |
| C、将AlCl3溶液滴入 NaOH 溶液中 |
| D、SO2通入BaCl2溶液中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com