
【题目】2005年10月12日北京时间上午9时,中国酒泉卫星发射中心成功将“神舟6号”飞船送入太空,这一壮举又一次受到世界关注.火箭推进器中有强还原剂液体肼(N2H4)和强氧化剂液态双氧水.当它们混合时,即产生大量氮气和水蒸气并放出大量热.已知:0.4mol液态肼与足量的液态双氧水反应生成氮气和水蒸气,放出256.652kJ的热量.
(1)反应的热化学方程
(2)又已知H2O(l)=H2O(g)△H=44kJ.mol﹣1 . 则16g液态肼与足量的液态双氧水反应生成氮气和液态水时放出的热量是kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外还有一个很大优点是 .
(4)燃料电池在航天器得到大量应用;科研人员新近开发出一种由甲醇、氧气以及强碱作电解质溶液的新型手机电池,充电一次可供手机连续使用一个月,据此请回答以下问题:
①甲醇是极,电极反应
②电池反应的离子方程式为 .
【答案】
(1)N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=﹣641.63kJ/mol
(2)408.815
(3)产物无污染
(4)负,CH3OH+8OH﹣﹣6e﹣═CO32﹣+6H2O,2CH3OH+3O2+4OH﹣═2CO32﹣+6H2O
【解析】解:(1)反应方程式为:N2H4+2H2O2═N2+4H2O,0.4mol液态肼放出256.652KJ的热量,则1mol液态肼放出的热量为 ![]() =641.63kJ,
=641.63kJ,
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.63kJ/mol;
(2)①N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.63kJ/mol;
②H2O(g)=H2O(l)△H=﹣44kJ/mol;
依据盖斯定律①+②×4得到:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l);△H=﹣817.63kJ/mol;
热化学方程式中32g全部反应放热817.63kJ,16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量为:817.63kJ× ![]() =408.815kJ;
=408.815kJ;
(3)还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,除释放大量热量和快速产生大量气体外,还有很突出的优点是,产物为氮气和水,清洁无污染;
(4)CH3OH和O2在电池中,肯定是O2氧化CH3OH,CH3OH是负极反应物,O2是正极反应物.CH3OH被氧化生成CO2和H2O,电解质溶液中有强碱(OH﹣),CO2要转化CO32﹣.
①甲醇是负极,电极反应式为:CH3OH+8OH﹣﹣6e﹣═CO32﹣+6H2O;
②CH3OH被氧化生成CO2和H2O,电解质溶液中有强碱(OH﹣),则CO2要转化CO32﹣,电池反应为:2CH3OH+3O2+4OH﹣═2CO32﹣+6H2O;
故答案为:(1)N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=﹣641.63kJ/mol;(2)408.815;(3)产物无污染;(4)①负;CH3OH+8OH﹣﹣6e﹣═CO32﹣+6H2O;②2CH3OH+3O2+4OH﹣═2CO32﹣+6H2O.
(1)根据题干信息确定1mol物质燃烧放出的热量,再得出反应的热化学方程式;
(2)根据盖斯定律确定反应放出的热量;
(3)燃烧产物是水和氮气,对大气无污染;
(4)在燃料电池中,燃料作为负极反应物,发生氧化反应;根据化合价变化确定得失电子数,再根据电荷守恒、原子守恒进行配平。


科目:高中化学 来源: 题型:
【题目】已知短周期主族元素Q、T、U、V、W、X、Y、Z原子序数依次增大。已知:T与U、V同周期,W与X、Y、Z同周期,U和Y同族;元素Q的某种核素没有中子;元素T的最高正价与最低负价的代数和为0;Q与U形成的气态化合物在标准状况下的密度为0.76g/L;工业上通过分离液态空气获得V的单质,且该单质的某种同素异形体是保护地球地表环境的重要屏障;W、X、Z的最高价氧化物对应的水化物两两之间都能反应,且W、X、Z原子最外层电子数之和等于W的原子序数。
(1)V元素原子的 L层电子数为______。元素 W 在周期表中的位置为______。
(2)用电子式表示化合物 QZ的形成过程______。
(3)U的氢化物比同主族其他元素的氢化物的熔沸点明显偏高,原因是______。
(4)写出X、Z 两种元素最高价氧化物对应的水化物相互反应的离子方程式:______。
(5)T、U、V形成的氢化物分子中共价键的极性由强到弱的顺序为______。(填化学式)
(6)Q与T可形成一种化合物T2Q4,请写出该分子的结构式________。
(7)元素Y的一种含氧酸化学式为 H3YO3,其结构式可表示为: 。该酸为______元酸,请写出该酸与过量氢氧化钠溶液反应的化学方程式______。(已知信息:氢氧原子结合成的一种原子团“—OH”叫羟基,含氧酸中只有羟基氢才可电离出 H+。)
。该酸为______元酸,请写出该酸与过量氢氧化钠溶液反应的化学方程式______。(已知信息:氢氧原子结合成的一种原子团“—OH”叫羟基,含氧酸中只有羟基氢才可电离出 H+。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应:2HI(g) ![]() H2(g)+I2(g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
H2(g)+I2(g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
A.HI、H2、I2的浓度相等
B.HI、H2、I2的浓度不再发生变化
C.HI、H2、I2在密闭容器中共存
D.容器内气体的颜色不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“观察DNA和RNA在细胞中的分布”实验中,使用盐酸的目的是 ( )
①改变细胞膜的流动性
②改变细胞膜的通透性
③改变细胞膜的化学组成
④将DNA与蛋白质分离
⑤将RNA与蛋白质分离
⑥利于RNA与染色剂结合
⑦利于蛋白质与染色剂结合
⑧利于DNA与染色剂结合
A.①④⑥ B.②④⑧ C.③⑤⑦ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1828年,德国化学家弗里德里希·维勒首次使用(NH4)2SO4与氰酸钾KCNO人工合成了尿素CO(NH2)2,打破了有机化合物的"生命力"学说。
(1) (NH4)2SO4与KCNO合成尿素反应的化学方程式为____________。
(2)某小组同学在实验室条件下,拟用CO2和NH3,在催化剂的作用下合成尿素。
①用CO2和NH3合成尿素 CO(NH2)2反应的化学方程式为____________。
②实验所需的CO2可用多种装置来制备,要想达到“随开随用、随关随停”的目的,下列装置A、B、C、D、E中符和要求的有____________(填字母)。
③若用F装置收集氨气,则气体应由导管口____________(填“a”或“b”)进入。




(3)尿素样品中氮含量可以用甲醛法标定,其原理如下:首先用浓硫酸分解试样,使试液中的胺生成硫酸铵并放出二氧化碳;将过量的硫酸中和后得到中性铵盐,再用甲醛(HCHO)与硫酸铵作用生成六次甲基四铵盐离子(CH2)6N4H+和硫酸;最后用标准氢氧化钠溶液滴定。
①甲醛与硫酸铵反应的离子方程式为____________;
②滴定选用的指示剂为____________。滴定终点的现象为____________。
③若称取样品m g,溶解后配成250mL溶液。取25.00mL样品溶液于250 mL锥形瓶中,加入10mL w%的甲醛溶液,充分反应后,加入1~2滴指示剂,用浓度为a mol/L的NaOH标准溶液滴定至终点(已知滴定时,1 mol六次甲基四铵盐离子(CH2)6N4H+消耗OH﹣的能力与1mol H+相当)。重复2次,消耗NaOH标准溶液的体积平均值为b mL。则该样品中氮的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)2NH2]氧化为环境友好物质形成的化学电源。当电池工作时,下列说法正确的是

A. 电子的流动方向M→Fe→CuSO4溶液→Cu-N
B. M极电极反应式: H2N(CH2)2NH2+16OH--16e-==2CO2↑+N2↑+12H2O
C. 当N极消耗5.6LO2时,则铁极增重32g
D. 一段时间后,乙中CuSO4溶液浓度基本保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.非金属元素之间构成的化合物都不是离子化合物
B.阴、阳离子通过静电引力所形成的化学键叫离子键
C.离子化合物中一定没有共价键
D.含有阳离子的化合物一定含有阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一体积不变的密闭容器中充入2mol A、0.6mol C和一定量的B三种气体,一定条件下发生反应2A(g)+B(g)3c(g),各物质的浓度随时间变化的关系如图1所示,其中如t0~t1阶段c(B)未画出.图2为反应体系中反应速率随时间变化的情况,且t2、t3、t4各改变一种不同的条件.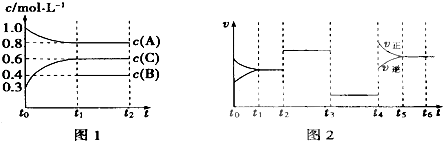
(1)若t1=15min,则t0~t1阶段以c的浓度变化表示的反应速率V(C)= .
(2)t3时改变的条件为 , B的起始物质的量为 .
(3)t4~t5阶段,若A的物质的量减少了0.01mol,而此阶段中反应体系吸收能量为a kJ,写出此条件下该反应的热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二醇(沸点:197.3℃)是一种重要的基础化工原料。由煤基合成气(主要成分CO、H2)与氧气先制备得到草酸二甲酯(沸点:164.5℃),再加氢间接合成乙二醇,具有反应条件温和、环境污染小等优点。反应过程如下:
反应I:4NO(g)+4CH3OH(g)+O2(g)![]() 4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
反应II:2CO(g)+2CH3ONO(g)![]() CH3OOCCOOCH3(l)+2NO(g) △H2=b kJ·mol-1
CH3OOCCOOCH3(l)+2NO(g) △H2=b kJ·mol-1
反应III:CH3OOCCOOCH3(1)+4H2(g)![]() HOCH2CH2OH(1)+2CH3OH(g)△H3 =c kJ·mol-1
HOCH2CH2OH(1)+2CH3OH(g)△H3 =c kJ·mol-1
请回答下列问题:
(1)煤基合成气间接合成乙二醇的总热化学方程式是_____________________________,已知该反应在较低温条件下能自发进行。说明该反应的△H ______0(填“>”“<”或“=”)。
(2)CO、CH3ONO各0.4mol在恒温、容积恒定为2L的密闭容器中发生反应II,达到平衡时CO的体积分数与NO的体积分数相等,计算该反应的化学平衡常数K=_____________。若此时向容器中再通入0.4molNO,一段时间后,达到新平衡时NO的体积分数与原平衡时相比______(填“增大”“相等”“减小”或“不能确定”)。
(3)温度改变对反应II的催化剂活性有影响,评价催化剂的活性参数——空时收率和CO的选择性可表示如下:
空时收率=CH3OOCCOOCH3质量/反应时间×催化剂的体积
CO的选择性=合成[CH3OOCCOOCH3所消耗的CO的物质的量/反应掉的CO的物质的量]×100%
在不同温度下,某学习小组对四组其他条件都相同的反应物进行研究,经过相同时间th,测得空时收率、CO的选择性数据如下表所示。
反应温度(℃) | 空时收率(g·mL-1·h-1) | CO的选择性(%) |
130 | 0.70 | ①72.5 |
140 | 0.75 | ②71.0 |
150 | 0.71 | ③55.6 |
160 | 0.66 | ④63.3 |
下列说法正确的是________(填字母代号)。
A.温度升高,空时收率先增大后减小,说明△H2>0
B.温度升高,催化剂活性逐渐减弱,对CO的选择性逐渐降低
C.综合考虑空时收率和CO的选择性,工业生成CH3OOCCOOCH3时,选择140℃效果最好
D.130℃时,CO的选择性最高,说明CO生成CH3OOCCOOCH3的转化率最高
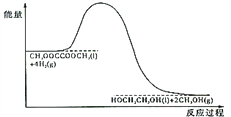
(4)120℃、常压时,CH3OOCCOOCH3+4H2![]() HOCH2CH2OH+2CH3OH反应过程中的能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中的能量变化图。________
HOCH2CH2OH+2CH3OH反应过程中的能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中的能量变化图。________
(5)研究证实,乙二醇、氧气可以在碱性溶液中形成燃料电池,负极的电极反应式是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com