
| ||
|
| 12.12×10-6mol |
| 30×10-3L |
|
| 1.79×10-10 |
| 2.00×10-5 |
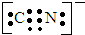 ,故答案为:
,故答案为: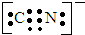 ;
;

科目:高中化学 来源: 题型:
| A、在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性 |
| B、向少量的火柴头浸泡液中滴加AgNO3、稀HNO3和NaNO2,检验火柴头中的氯元素 |
| C、在2mL紫色的CoCl2溶液中加入浓盐酸,可使溶液显蓝色 |
| D、制备摩尔盐时,最后在蒸发皿中蒸发浓缩溶液,加热至液体表面出现晶膜为止,不能将溶液全部蒸干 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在容积固定为2L的密闭容器中,充入0.18molHI,480℃时反应:
在容积固定为2L的密闭容器中,充入0.18molHI,480℃时反应:| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
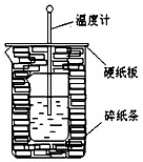
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气通入硝酸银溶液中:Cl2+H2O+Ag+→AgCl↓+H++HClO |
| B、用硫酸铜溶液吸收硫化氢气体:Cu2++S2-→CuS↓ |
| C、次氯酸钠溶液中通入少量二氧化碳:ClO-+H2O+CO2→HCO3-+HClO |
| D、向NaHCO3溶液中加入少量的Ba(OH)2溶液:Ba2++2HCO3-+2OH-→BaCO3↓+CO32-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com