
【题目】下列溶液中Cl-浓度最大的 ( )
A.200mL 2mol/L MgCl2溶液B.1000mL 2.5mol/L NaCl溶液
C.250mL 1mol/L AlCl3溶液D.200mL 4.5mol/L KClO3溶液
科目:高中化学 来源: 题型:
【题目】(1)有以下6个反应(反应条件略):
A.2Na+2H2O ═2NaOH+H2↑ B.CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
C.KClO3![]() 2KCl+3O2↑ D.CaCO3+2HCl═CaCl2+H2O+CO2↑
2KCl+3O2↑ D.CaCO3+2HCl═CaCl2+H2O+CO2↑
E.Na2O+CO2 ═Na2CO3 F.CO2+C![]() 2CO
2CO
既属于化合反应又属于氧化还原反应的有__________(填编号,下同),不属于氧化还原反应的有__________.
(2)根据反应:①2Fe3++2I-===2Fe2++I2,②Br2+2Fe2+===2Fe3++2Br-,③ Br2+2I-===I2+2Br-,回答下列问题。
①试判断离子的还原性由强到弱的顺序是________
A.Br-、Fe2+、I- B.I-、Fe2+、Br- C.Br-、I-、Fe2+ D.Fe2+、I-、Br-
②某溶液中含有Br-、Fe2+、I-,为了氧化I-而不影响Br-和Fe2+,选用的氧化剂是__________;
③I2与Br-能否发生反应________
A.能 B.不能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种医药中间体,常用于制备抗凝血药。可以通过如图所示的路线合成:
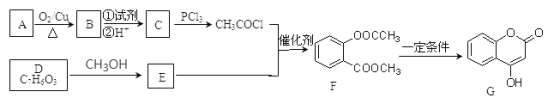
已知:①RCOOH![]() RCOCl;②D与FeCl3溶液能发生显色反应。
RCOCl;②D与FeCl3溶液能发生显色反应。
③:![]()
回答下列问题:
(1)C→H的反应类型是_______________,B→C步骤①中所加的试剂可能是_____________,D中的官能团名称为____________________。
(2)B、E的结构简式为:B:_____________,E:______________。
(3)A→B的化学方程式为_________________,G与足量NaOH溶液充分反应的化学方程式为_________________________。
(4)写出同时满足下列条件的所有E的同分异构体的结构简式________________。
①不能发生水解反应,能发生银镜反应
②该分子核磁共振氢谱有五个组峰,且峰面积之比为2:2:2:1:1
③与FeCl3溶液能发生显色反应
④苯环上有两种不同化学环境的氢原子
(5)已知:酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯(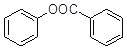 )是一种重要的有机合成中间体。试结合题中信息写出以苯酚、甲苯为原料制取该化合物合成路线流程图(其他试剂任选)______。合成路线流程图示例:
)是一种重要的有机合成中间体。试结合题中信息写出以苯酚、甲苯为原料制取该化合物合成路线流程图(其他试剂任选)______。合成路线流程图示例: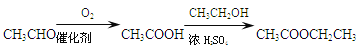
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关油脂的说法错误的是
A. 植物油兼有酯类和烯烃的性质
B. 油脂的水解叫皂化反应
C. 液态油催化加氢后可以生成固态脂肪
D. 脂肪里的饱和烃基的相对含量较大,熔点较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的部分框架,请回答:

(1)根据元素周期表回答下面问题:
(a)写出元素⑥在周期表中的位置___________;元素⑦和元素⑧的最高价氧化物的水化物中酸性较强是___________(用化学式表示)。
(b)元素②与元素⑨形成的化合物属于___________(填“共价”或“离子”,下同)化合物.元素⑤与元素⑨形成的化合物属于___________化合物。
(c)请写出元素②的原子结构示意图为___________;元素②的最高价氧化物结构式为:___________;元素①﹣④中的某单质在常温下化学性质稳定,通常可以做保护气,请用电子式表示其分子___________。
(2)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线法则.根据元素周期表对角线法则,金属铍(Be)与铝单质及其化合物性质十分相似.
(a)写出证明Al2O3是两性物质的化学反应的离子方程式:___________,___________。
(b)下列关于铍的判断正确的是__________
A.氧化铍的化学式为Be2O3 B.Be(OH)2可溶于水
C.BeCl2是离子化合物 D.Be(OH)2具有两性
(c)Be(OH)2和Mg(OH)2可用试剂___________鉴别。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素。稀土元素有“工业维生素”的美称,如今已成为极其重要的战略资源。
(1)钪(Sc)为21号元素,位于周期表的_____区,基态原子价电子排布图为_______。
(2)离子化合物Na3[Sc(OH)6]中,存在的化学键除离子键外还有_______。
(3)Sm(钐)的单质与l,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+CH2=CH2。
ICH2CH2I中碳原子杂化轨道类型为______, lmol CH2=CH2中含有的σ键数目为______。常温下l,2-二碘乙烷为液体而乙烷为气体,其主要原因是__________。
(4) PrO2(二氧化镨)的晶体结构与CaF2相似,晶饱中Pr(镨)原子位于面心和顶点。则PrO2(二氧化镨)的晶胞中有________个氧原子。
(5)Ce(铈)单质为面心立方晶体,其晶胞参数a=516pm。晶胞中Ce(铈)原子的配位数为_______,列式表示Ce(铈)单质的密度:________g/cm3(用NA表示阿伏伽德罗常数的值,不必计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过CO传感器可监测CO的含量,总反应为2K2FeO4+3CO+2KOH+2H2O=2Fe(OH)3+3K2CO3,其工作原理示意图如下,下列说法正确的是
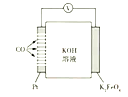
A. 电极为负极,可以用Fe电极代替
B. 工作时OH-向K2FeO4电极移动
C. 每转化3molCO,有2molK2FeO4被氧化
D. K2FeO4电极上的电极反应式是2FeO42-+8H2O+6e-=2Fe(OH)3↓+10OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,X与M同主族,Z的气态氧化物能与其最高价氧化物的水化物反应,G是地壳中含量最高的金属元素。清回答下列问题:
(1)Q的元素符号为______,Y、Z、M、G四种元素原子半径由大到小的顺序是(写元素符号)___________。
(2)Y在元素周期表中的位置为_______________,Y与硫元素形成的二元化合物的电子式为_________________________。
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)____________________。
(4)单质Y和元素Z的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为_________。
(5)Z和G组成的化合物GZ,被大量用于制造电子元件。工业上用G的氧化物、Y单质和Z单质在高温下制备GZ,其中G的氧化物和Y单质的物质的量之比为1:3,则该反应的化学方程式为__________________________。
(6)常温下,不能与G的单质发生反应的是(填序号)_________________________。
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学中常见的四种不同微粒,它们之间存在如图所示的转化关系。
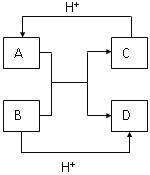
(1)如果A、B、C、D均是10电子微粒,请写出A的化学式:___________;D的化学式__________。
(2)如果A和C是18电子的微粒,B和D是10电子的微粒,请写出A与B在溶液中反应的离子方程式:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com