
| A. | 草酸与氢氧化钠溶液混合呈中性时,溶液中存在:c(Na+)=c(HC2O4-)+c(C2O42-) | |
| B. | NaHC2O4与NaClO溶液混合,反应的离子方程式为:HC2O4-+ClO-=HClO+C2O42- | |
| C. | (NH4)2C2O4溶液中:c(NH4+)=2 c(H2C2O4)+2 c(HC2O4-)+2 c(C2O42-) | |
| D. | 草酸使酸性KMnO4溶液褪色,离子方程式为:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O |
分析 A.中性时是NaHC2O4和Na2C2O4的混合物,依据溶液中存在电荷守恒解答;
B.草酸具有还原性能被次氯酸根离子氧化;
C.氨根离子存在水解;
D.草酸具有还原性能够被高锰酸钾氧化.
解答 解:A.中性时是NaHC2O4和Na2C2O4的混合物,由电荷守恒知C(H+)+C(Na+)=C(HC2O4-)+2c(C2O42-),+C(OH-),由于溶液呈中性,所以H+=OH-,c(Na+)=c(HC2O4-)+2c(C2O42-),故A错误;
B.NaHC2O4与NaClO溶液混合,反应的离子方程式为:HC2O4-+ClO-=HCO3-+CO2↑+Cl-,故B错误;
C.NH4+也会水解,依据原子个数守恒可知:C(NH3)+c(NH4+)=2 c(H2C2O4)+2 c(HC2O4-)+2 c(C2O42-),故C错误;
D.草酸使酸性KMnO4溶液褪色,离子方程式为:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确强酸制备弱酸的规律、次氯酸根的强氧化性、溶液中存在的守恒规律是解题关键,题目难度中等.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 5.6g金属铁于足量的盐酸反应,转移电子数为0.2NA | |
| B. | 标准状况下,以任意比混合的H2、CO2的混合气体22.4L,所含分子数为NA | |
| C. | 含NA个Na+的Na2O2溶于1L水中,溶质的物质的量浓度为1mol•L-1 | |
| D. | 20g重水(D2O)所含的电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 近年来AIST报告正在研制一种“高容量、低成本”锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )
近年来AIST报告正在研制一种“高容量、低成本”锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )| A. | 放电时,Li+透过固体电解质向Cu极移动 | |
| B. | 若负载为铅蓄电池,则在对铅蓄电池充电时与Cu极相连的一极发生还原反应. | |
| C. | 通空气时时,正极的电极反应式为Cu2O+H2O+2e-=2Cu+2OH- | |
| D. | 整个反应过程中,铜相当于催化剂. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑥ | B. | ①③④⑤ | C. | ②③⑤ | D. | ①②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 杭州市萧山区红山农场近期完成了天然气管道安装,从此每家每户结束液化煤气使用时代,这一举措有利于降低氮氧化合物的排放 | |
| B. | 电动汽车、甲醇燃料汽车的出现,有利于节能减排,保护环境 | |
| C. | 利用天阳能等清洁能源代替化石燃料,有利于节约资源,造福后代 | |
| D. | 2015年春节期间,烟花爆竹的燃放时间比往年减少一天,市民也自觉减少烟花的燃放量,这有利于减少雾霾天气的出现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 | |
| B. | 在含有BaSO4沉淀的溶液中加人Na2SO4固体,c(Ba2+)增大 | |
| C. | 含1molKOH的溶液与lmolCO2完全反应后,溶液中c(K+ )=c (HCO3- ) | |
| D. | 改变条件使醋酸溶液中的醋酸根离子浓度增大,溶液的pH值可能减小也可能增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、基态Z原子的价层电子排布图
、基态Z原子的价层电子排布图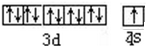 .从光谱的角度解释Z原子特征焰色产生原因:铜原子的外层电子在发生跃迁时会一定波长的光
.从光谱的角度解释Z原子特征焰色产生原因:铜原子的外层电子在发生跃迁时会一定波长的光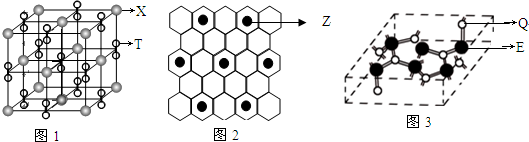
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作及现象 | 现象的解释 | |
| A | 将一片铝箔置于酒精灯外焰上灼烧,铝箔熔化但不滴落 | 单质铝的熔点特别高 |
| B | 用玻璃尖嘴导管导出氢气,点燃,观察到火焰呈黄色 | 普通玻璃中含有钠元素 |
| C | 往水中加入Na2O2固体,滴入酚酞呈红色,振荡,红色褪去 | 产生了碱性物质,且Na2O2具有漂白性 |
| D | 向过量的苯酚浓溶液中滴加少许饱和溴水,振荡,未观察到白色沉淀产生 | 三溴苯酚溶解在过量的苯酚中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com