
【题目】下列变化属于化学变化的是
A.过滤B.蒸馏C.氧化D.分液
科目:高中化学 来源: 题型:
【题目】在通常条件下,NO2和SO2可以很容易发生反应生成NO和SO3 . 现将碳跟浓硫酸共热产生的气体X和碳跟浓硝酸共热产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( ) 
A.洗气瓶中产生的沉淀是碳酸钡
B.洗气瓶中产生的沉淀是硫酸钡
C.在Z导管出来的气体中无二氧化碳
D.反应一段时间后洗气瓶中溶液的酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中能证明碳的非金属性比硅强的是( ) ①往Na2SiO3溶液中通入CO2产生白色沉淀
②石墨是导体,晶体硅是半导体
③制玻璃过程中发生反应Na2CO3+SiO2 ![]() Na2SiO3+CO2↑
Na2SiO3+CO2↑
④CH4比SiH4稳定.
A.①④
B.②③
C.③④
D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于烯烃、炔烃的叙述中,正确的是
A. 某物质的名称为2-乙基-1-丁烯,它的结构简式为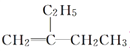
B. CH3—CH===CH—C≡C—CF3分子结构中6个碳原子可能都在一条直线上
C. 相同物质的量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的量相同
D. β—月桂烯的结构如图![]() 所示,该物质与等物质的量溴发生加成反应的产物(不考虑立体异构)理论上最多有5种
所示,该物质与等物质的量溴发生加成反应的产物(不考虑立体异构)理论上最多有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高分子化合物R的结构简式如图,下列有关R的说法正确的是

A. R的单体之一的分子式为C9H10O2
B. R完全水解后生成物均为小分子有机物
C. 碱性条件下,1molR完全水解消耗NaOH的物质的量为2mol
D. 通过加聚反应和缩聚反应可以生成R
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为 .
(2)表中元素原子半径最大的是(写元素符号) .
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是 .
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1mol X的最高价化合物,恢复至室温,放热687kJ.已知该化合物的熔、沸点分别为﹣69℃和58℃.写出该反应的热化学方程式: .
(5)碳与镁生成的1mol化合物Q与水反应生成2mol Mg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为 . Q与水反应的化学方程式为 .
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50,为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2molL﹣1 NaOH溶液和1mol O2 , 则两种气体的分子式及物质的量分别为 , 生成硫酸铜物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的溶液是高中化学一个重要实验.实验室要配制1mol/L的稀硫酸溶液100mL,回答下列有关问题:
(1)配制时,必须用到下列仪器中的 . 
(2)配制时两次用到玻璃棒,两次的作用分别是和 .
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次);A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.用一定规格的量筒准确量取所需浓硫酸的体积,缓缓注入水中,用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的溶液沿玻璃棒注入100mL的容量瓶中
D.将容量瓶盖紧,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)配制过程中出现以下情况,使所配溶液浓度偏低的有(填代号).①没有洗涤烧杯和玻璃棒.②如果加水超过了刻度线,取出水使液面恰好到刻度线.③容量瓶没有干燥.④定容时仰视刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com