
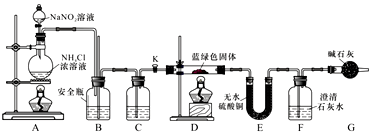
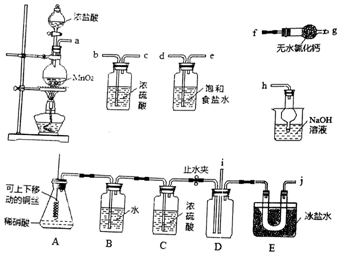
分析 A装置制备氮气排除装置中的空气,B作安全瓶,C干燥生成的氮气,装置D分解碱式碳酸铜[xCuCO3•yCu(OH)2],盛放无水硫酸铜的E装置吸收分解生成的水分,F吸收分解生成的二氧化碳,用G装置吸收空气中水蒸气和二氧化碳,防止干扰实验,
(1)铜离子水解,加酸抑制其水解,根据溶质质量分数=$\frac{溶质的质量}{溶液的质量}×100%$计算;
(2)加热亚硝酸钠和氯化铵混合溶液生成N2和氯化钠;
(3)通入N2的目的是排除装置中的空气;B装置中当装置内压力过大时,B瓶中间的安全管中液面上升,使压力稳定,作安全瓶;C瓶干燥气体;
(4)加热D后生成黑色的氧化铜,水分使无水硫酸铜显蓝色,二氧化碳使澄清石灰石变浑浊,故现象为:硬质玻璃管中蓝绿色固体变黑色,E中白色固体变蓝,F中溶液变浑浊;
(5)Ca(OH)2为微溶物,溶解度比Ba(OH)2小,Ksp[CaCO3]=2.8×10-9,Ksp[BaCO3]=5.1×10-9,均为难溶物,且溶解度相差不大,据此分析;
(6)待D中反应完全后,打开活塞K,再次滴加NaNO2溶液产生N2,其目的是让停留在装置中的气体被充分吸收,减小实验误差;E中吸收的是水,F中吸收的是二氧化碳,根据质量守恒定律测得氧化铜的质量,根据原子守恒确定其化学式.
解答 解:(1)铜离子水解,加酸抑制其水解;
12.5 g胆矾中含有硫酸铜的质量为12.5×$\frac{160}{160+90}$=8g,
87.4 mL蒸馏水的质量为87.4g,则溶液的质量为12.5g+87.4g=99.9g,
所得硫酸铜溶液的溶质质量分数为$\frac{8g}{99.9}×100%$=8%;
故答案为:抑制Cu2+水解,防止溶液变浑浊;8.0%;
(2)加热亚硝酸钠和氯化铵混合溶液生成N2和氯化钠,化学方程式为:NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+N2↑+2H2O;
故答案为:NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+N2↑+2H2O;
(3)通入N2的目的是排除装置中的空气,B装置中当装置内压力过大时,B瓶中间的安全管中液面上升,使压力稳定,作安全瓶;C瓶装浓硫酸干燥氮气;
故答案为:排除装置中的空气;当装置内压力过大时,B瓶中间的安全管中液面上升,使压力稳定;浓硫酸;
(4)加热D后生成黑色的氧化铜,水分使无水硫酸铜显蓝色,二氧化碳使澄清石灰石变浑浊,故现象为:硬质玻璃管中蓝绿色固体变黑色,E中白色固体变蓝,F中溶液变浑浊;
故答案为:硬质玻璃管中蓝绿色固体变黑色,E中白色固体变蓝,F中溶液变浑浊;
(5)Ba(OH)2溶解度大于Ca(OH)2,充分吸收CO2,BaCO3的摩尔质量大于CaCO3,测量误差小;氢氧化钙为强碱,CaCO3的溶解度和BaCO3溶解度相差不大;
故答案为:bd;
(6)待D中反应完全后,打开活塞K,再次滴加NaNO2溶液产生N2,其目的是让停留在装置中的气体被充分吸收,减小实验误差;
E中吸收的是水,水的物质的量为$\frac{0.27g}{18g/mol}$=0.015mol,F中吸收的是二氧化碳生成碳酸钡白色沉淀,根据碳原子守恒得二氧化碳的物质的量为$\frac{1.97g}{197g/mol}$=0.01mol,氧化铜的物质的量=(2.71g-0.27g-0.01mol×44g/mol)÷80g/mol═0.025mol,则铜离子、氢氧根离子和碳酸根离子的物质的量之比=0.025mol:0.03mol:0.01mol=5:6:2,所以其化学式为:2CuCO3•3Cu(OH)2;
故答案为:让停留在装置中的气体被充分吸收,减小实验误差;2CuCO3•3Cu(OH)2.
点评 本题以物质制备为载体,考查学生对原理的分析理解、物质含量测定等,难点是化学式的确定,需要学生具备扎实的基础,题目难度中等.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 7.1gCl2与足量NaOH溶液反应转移0.2×6.02×1023个电子 | |
| B. | 1mol羟基中含有的电子数目为9×6.02×1023个 | |
| C. | 标准状况下,2.24L辛烷含有0.8×6.02×1023个碳原子 | |
| D. | 1L 0.50mol/L Na2CO3溶液中含有1.5×6.02×1023个离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol H2O的质量为36g/mol | |
| B. | NH3的摩尔质量为17g | |
| C. | 3.01×1023个SO2分子的质量为32g | |
| D. | 标准状况下,3 mol任何物质体积均为67.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2+3H2=2NH3属于自然固氮 | |
| B. | 固氮属于氧化还原反应 | |
| C. | 俗语“雷雨发庄稼”毫无科学道理 | |
| D. | 氨气溶于水得到的溶液能导电,所以NH3是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
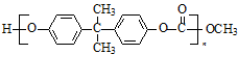

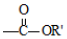 +
+ $\stackrel{H+}{→}$
$\stackrel{H+}{→}$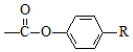 +HOR′
+HOR′ .
.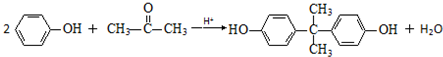 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{电解}{→}$Mg | |
| B. | 由NaCl制漂白剂:NaCl(aq)$\stackrel{电解}{→}$Cl2$\stackrel{石灰乳}{→}$漂白粉 | |
| C. | 由铝土矿冶炼铝:铝土矿$→_{Na_{3}AlF_{6}}^{电解}$Al | |
| D. | 合成NH3:NH4Cl和Ca(OH)2固体$\stackrel{△}{→}$NH3$\stackrel{碱石灰}{→}$纯净干燥的氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
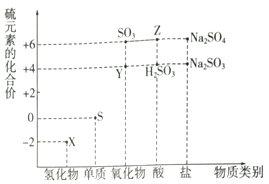 利用元素的化合价推测物质的性质是化学研究的重要手段.
利用元素的化合价推测物质的性质是化学研究的重要手段.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,这是利用了KNO3的氧化性 | |
| B. | 我国古代文献《天工开物》记载“凡研硝(KNO3)不以铁碾入石臼,相激火生,祸不可测”,这是因为KNO3能自燃 | |
| C. | 《本草经集注》中记载了区分硝石(KNO3)和朴硝(Na2SO4)的方法:“以火烧之,紫青烟起,乃真硝石也”,这是利用了焰色反应 | |
| D. | 西汉时期的《淮南万毕术》中有“曾青得铁,则化为铜”的记载,所涉及的化学反应为:Fe+CuSO4═FeSO4+Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com