
| A、麦芽糖与蔗糖的水解产物均为葡萄糖,且均为二糖 |
| B、加热能杀死流感病毒是因为病毒的蛋白质受热变性 |
| C、赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色 |
| D、乙烯、氯乙烯、苯乙烯都是不饱和烃,均可用于合成有机高分子材料 |


科目:高中化学 来源: 题型:

| A、a+b>c+d T1<T2 Q<0 |
| B、a+b>c+d T1>T2 Q>0 |
| C、a+b<c+d T1>T2 Q>0 |
| D、a+b>c+d T1>T2 Q<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2的燃烧热为285.8 kJ/mol | ||
B、H2和O2反应生成液态水时的热化学方程式为H2(g)+
| ||
| C、稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ | ||
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
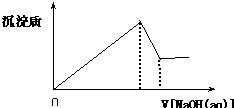 向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则该溶液中可能存在的离子是( )
向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则该溶液中可能存在的离子是( )| A、只有Mg2+ |
| B、只有Al3+ |
| C、有H+、Mg2+和Al3+ |
| D、有Mg2+和Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①② |
| C、只有③ | D、全部错误 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,将22.4L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA |
| B、常温常压下,16g14CH4所含中子数目为8NA |
| C、常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA |
| D、标准状况下,22.4L空气含有NA个单质分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
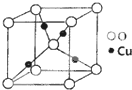 某催化剂中含有的活性组分为Ni、Cu和Zn的化合物,可用于二氧化碳加氢制取甲醚.甲醚是乙醇的同分异构体,其熔点-141.5℃,沸点-24.9℃,在加热条件下可分解成甲烷、乙烷、甲醛等.
某催化剂中含有的活性组分为Ni、Cu和Zn的化合物,可用于二氧化碳加氢制取甲醚.甲醚是乙醇的同分异构体,其熔点-141.5℃,沸点-24.9℃,在加热条件下可分解成甲烷、乙烷、甲醛等.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com