
| A. | 与同族硅元素类似,锗、锡、铅都可用做半导体材料 | |
| B. | 锗与盐酸可能不反应,锡、铅能与盐酸反应 | |
| C. | 锗、锡、铅的+4价氢氧化物的碱性由弱到强的顺序为:Ge(OH)4<Sn(OH)4<Pb(OH)4 | |
| D. | 锗、锡、铅的金属性依次减弱 |
分析 A、在金属和非金属性元素的交界处的单质能作半导体材料;
B、锗与硅的性质相似,与盐酸不反应,锡、铅在金属活动顺序表中排在氢的前面,能与盐酸反应;
C、根据金属性越强,对应最高价氧化物的水化物的碱性越强分析;
D、根据同主族金属性的变化规律分析.
解答 解:A、在金属和非金属性元素的交界处的单质能作半导体材料,硅、锗都位于金属与非金属的交界处,都可以做半导体材料,而锡、铅不是半导体,故A错误;
B、锗与硅的单质都能作半导体,化学性质相似,所以与盐酸不反应,锡、铅在金属活动顺序表中排在氢的前面,能与盐酸反应,故B正确;
C、同主族从上到下金属性增强,所以锗、锡、铅的金属性依次增强,则其对应最高价氧化物的水化物的碱性依次增强,碱性:Ge(OH)4<Sn(OH)4<Pb(OH)4,故C正确;
D、同主族从上到下金属性增强,所以锗、锡、铅的金属性依次增强,故D错误.
故选AD.
点评 本题考查了同主族元素性质的递变规律,注意根据元素周期律分析,侧重金属元素的性质的考查,题目难度不大.


科目:高中化学 来源: 题型:推断题
| 实验操作 | 预期现象 | 结论 | |
| 验证猜想Ⅰ | 步骤①:取少量0.01mol/L酸性KMnO4溶液,滴入所得溶液 | 溶液紫红色褪去 | 含有Fe2+(或溶液紫红色不褪去,不含Fe2+) |
| 步骤②:另取少量所得溶液,滴加KI-淀粉溶液 | 含有Fe3+ | ||
| 验证猜想Ⅱ | 将所得气体通入如图装置: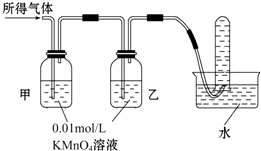 | 甲中KMnO4溶液褪色,乙中KMnO4溶液颜色不变,试管中收集到气体 | 含有两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA | |
| B. | NA个Fe(OH)3胶体粒子的质量为107g | |
| C. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| D. | 2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0.2NA之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0 项 | B. | 1 项 | C. | 2 项 | D. | 3 项 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.0004mol/(L•min) | B. | 0.0002mol/(L•s) | C. | 0.0016 | D. | 0.012 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ③④ | C. | ①② | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:实验题
某化工厂用软锰矿(含MnO2及少量Al2O3)和闪锌矿(含ZnS及少量FeS)联合生产Zn、MnO2,其部分生产流程如下:
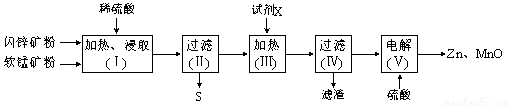
已知:过滤(Ⅱ)所得滤液是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Zn(OH)2 | Mn(OH)2 |
开始沉淀时的pH | 2.7 | 4.0 | 6.4 | 7.7 |
完全沉淀时的pH | 3.7 | 5.2 | 8.0 | 10.4 |
(1)加热、浸取时所加矿石均需粉碎,其目的是 。
(2)写出FeS和MnO2和稀硫酸反应的离子方程式: 。
(3)试剂X的作用是调节溶液的pH以生成Fe(OH)3、Al(OH)3。pH调节的范围是 ,试剂X可以选用 (填选项字母)。
A.MnCO3 B.Na2CO3 C.Zn2(OH)2CO3 D.NH3·H2O
(4)电解(Ⅴ)中阳极的电极反应式为 。
(5)Zn和MnO2是制作电池的原料。某锌-锰碱性电池以KOH溶液为电解质溶液,其电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。该电池的正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径 (10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | 1.02 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6 | +1 | |
| -2 | -3 | -1 | -3 | -2 |
 ;
;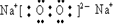 .
. ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com