
【题目】铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等,回答下列问题:
(1)铅与碳是同族元素,则下列说法正确的是 .
a.主要化合价为+2,+4
b.同族的Si与Ge(锗)均为半导体材料,铅也为半导体材料.
c.铅的最高价氧化物对应水化物的酸性强于碳酸
d.与同族的Ge(锗)作比较:碱性Ge(OH)4<Pb(OH)4 , 则金属性Ge<Pb,周期表中位置Pb在Ge下面.
e.同族的Ge(锗)与盐酸不反应,Pb与盐酸能反应,则原子半径Ge>Pb
(2)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为 .
(3)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
2PbS(s)+3O2(g)=2PbO(s)+2SO2(g)△H=a kJmol﹣1
PbS(s)+2PbO(s)=3Pb(s)+SO2(g)△H=b kJmol﹣1
PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g)△H=c kJmol﹣1
反应3PbS(s)+6O2(g)=3PbSO4(s)△H=kJmol﹣1(用含a,b,c的代数式表示).
(4)引爆导弹、核武器的工作电源通常Ca/PbSO4热电池,其装置如图1所示,该电池正极的电极反应式为 . 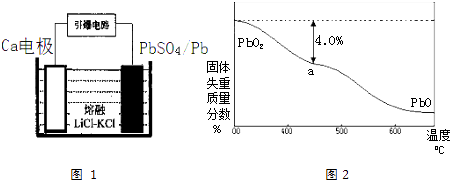
(5)PbO2在加热过程发生分解的失重曲线如图2所示,已知失重曲线上的a点为样品失重4.0%[即:( ![]() ×100%]的残留固体.若a点固体组成表示为PbOx或mPbO2nPbO,列式计算x值 , 和m:n值 .
×100%]的残留固体.若a点固体组成表示为PbOx或mPbO2nPbO,列式计算x值 , 和m:n值 .
【答案】
(1)ad
(2)PbO+ClO﹣=PbO2+Cl﹣
(3)2a+2b﹣3c
(4)PbSO4+2e﹣=SO42﹣+Pb
(5)1.4;2:3
【解析】解:(1.)a.铅与碳是同族元素,最外层电子数为4,主要化合价为+2、+4,故a正确;b.同族的Si与Ge(锗)均为半导体材料,铅是金属不是半导体材料,故b错误;c.同主族最高价氧化物对应水化物形成的酸性减弱,铅的最高价氧化物对应水化物的酸性弱于碳酸,故c错误;d.同主族从上到下金属性增强,形成最高价氢氧化物的碱性增强,与同族的Ge(锗)作比较:碱性Ge(OH)4<Pb(OH)4 , 则金属性Ge<Pb,周期表中位置Pb在Ge下面,故d正确;e.同族的Ge(锗)与盐酸反应,Pb与盐酸能反应,则原子半径Ge<Pb,故e错误;所以答案是:ad;
(2.)PbO和次氯酸钠反应生成二氧化铅和氯化钠,离子方程式为PbO+ClO﹣=PbO2+Cl﹣ , 所以答案是:PbO+ClO﹣=PbO2+Cl﹣;
(3.)已知:①2PbS(s)+3O2(g)=2PbO(s)+2SO2(g)△H=a kJmol﹣1②PbS(s)+2PbO(s)=3Pb(s)+SO2(g)△H=b kJmol﹣1③PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g)△H=c kJmol﹣1
将①×2+②×2﹣③×3可得反应3PbS(s)+6O2(g)=3PbSO4(s)
根据盖斯定律△H=2△H1+2△H2﹣3△H3=(2a+2b﹣3c)kJmol﹣1所以答案是:2a+2b﹣3c;
(4.)根据装置图,判断正极为PbSO4发生还原反应,所以答案是PbSO4+2e﹣=SO42﹣+Pb,所以答案是:PbSO4+2e﹣=SO42﹣+Pb;
(5.)若a点固体组成表示为PbOx , 根据PbO2 ![]() PbOx+
PbOx+ ![]() O2↑,
O2↑, ![]() ×32=239×4.0%,x=1.4;若组成为mPbO2nPbO,根据原子守恒得,O原子和Pb原子的比值=x=
×32=239×4.0%,x=1.4;若组成为mPbO2nPbO,根据原子守恒得,O原子和Pb原子的比值=x= ![]() =1.4,得m:n=2:3,所以答案是:1.4;2:3;
=1.4,得m:n=2:3,所以答案是:1.4;2:3;


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】将乳清蛋白、淀粉、胃蛋白酶、唾液淀粉酶和适量水混合装入一个容器内,调整pH至2.0,保存于37℃的水溶锅中,过一段时间后,容器内剩余的物质是
A.淀粉、胃蛋白酶、多肽、水
B.唾液淀粉酶、淀粉、胃蛋白酶、水
C.唾液淀粉酶、胃蛋白酶、多肽、水
D.唾液淀粉酶、麦芽糖、胃蛋白酶、多肽、水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组选用下列装置和药品制取纯净乙炔并进行有关乙炔性质的探究,试回答下列问题。
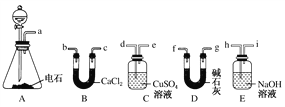
(1)A中制取乙炔的化学方程式为_________________________________。
(2)制乙炔时,旋开分液漏斗的活塞,使水慢慢滴下的原因是_________________。
(3)用电石制得的乙炔中常含有H2S、PH3等杂质,除去杂质应选用________(填序号,下同)装置,干燥乙炔最好选用________装置。
(4)为了探究乙炔与HBr发生加成反应后的有关产物,进行以下实验:
纯净乙炔气![]() 混合液
混合液![]() 有机混合物Ⅰ
有机混合物Ⅰ![]() 混合液
混合液![]() 有机混合物Ⅱ
有机混合物Ⅱ
①操作b的名称是________;
②有机混合物Ⅰ可能含有的物质是________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的有几个装置( ) 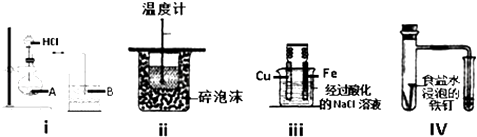
①在装置i的烧瓶A中装入饱和碳酸钠溶液,在烧杯B中装入水玻璃(硅酸钠溶液),可以证明非金属性:Cl>C>Si
②在装置i的烧瓶A中装入饱和碳酸钠溶液,在烧杯B中装入水玻璃(硅酸钠溶液),可以证明酸性:HCl>H2CO3>H2SiO3
③装置ii可以测定酸碱中和热
④装置iii在保护金属Fe,是牺牲阳极的阴极保护法
⑤装置IV可验证铁的吸氧腐蚀实验.
A.1个
B.2个
C.3个
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是18×7的格子,按要求作答
A | He | ||||||||||||||||
G | C | D | |||||||||||||||
B | E | F | I | H | |||||||||||||
Fe | Cu | ||||||||||||||||
(1)用封闭的实线绘出元素周期表的轮廓,注意:不得使用铅笔作图.
(2)C元素的一种中子数为10的同位素的原子符号为 , C2﹣的离子结构示意图为 , C,D,E,F的简单离子半径由小到大顺序是 . (填写离子符号 )
(3)A,G,C中的2种或3种元素能形成18个电子的分子、(填化学式),其中A,G也能形成GA5的离子化合物(填电子式).
(4)请分别用1个离子方程式说明B和F的金属性强弱: , C和D的非金属性强弱 .
(5)Fe位于周期表周期族,请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱.写出总反应式:负极电极反应式: , 并在方框内画出实验装置图,并标注电极材料和电解质溶液. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类的说法正确的是( )
A.糖类都有甜味,其通式为CnH2mOm
B.纤维素水解的最终产物是互为同分异构体的葡萄糖和果糖
C.只用银镜反应能判断淀粉水解是否完全
D.淀粉和纤维素都属于多糖类天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验可实现鉴别目的的是( )
A. 用稀硫酸鉴别两种金属银和铝
B. 用硝酸银溶液鉴别氯化钾溶液和氯化钠溶液
C. 用二氧化碳鉴别氢氧化钠溶液和氯化钠溶液
D. 用氯化钡溶液鉴别硝酸银溶液和碳酸钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为常见气体制备、干燥、性质验证和尾气处理的部分仪器装置(加热及固定装置均略去),仪器装置可任意选择,必要时可重复选用。

请回答下列问题:
(1)若在装置A的烧瓶中装入锌片,分液漏斗中装入稀硫酸,以验证H2的还原性并检验其氧化产物。按___C顺序连接,装置B中所盛放药品的化学式____(填化学式)。
(2)若在装置A的烧瓶中装入Na2O2,分液漏斗中装入浓氨水,装置B中装入固体催化剂,以进行氨的催化氧化。若装置的连接顺序为A→C→B→C,则装置B中氨的催化氧化反应的化学方程为________装置B中可能观察到的现象是__________。
(3)若在装置A的烧瓶中装入Na2SO3,分液漏斗中装入浓H2SO4,装置B中装入Na2O2,以探究SO2气体与Na2O2反应。装置连接的顺序为A→____→_____→___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com