
| A. | 标准状况下,5.6L NO和5.6L O2混合后的分子总数为0.5NA | |
| B. | 25g 质量分数为68%的H2O2水溶液中含氧原子数目为NA | |
| C. | 高温下,16.8g Fe 与足量水蒸气完全反应失去0.8NA个电子 | |
| D. | 1mol CH5+中含有的电子数目为11NA |
分析 A、在NO2气体中存在平衡:2NO2?N2O4,导致气体体积偏小;
B.双氧水和水都含有氧原子;
C.n=$\frac{m}{M}$计算得到物质的量,结合铁和水蒸气反应生成四氧化三铁和氢气,计算电子转移数;
D.一个CH5+中含有的电子数为10.
解答 解:A、一氧化氮和氧气不需要任何条件即可反应,由2NO+O2═2NO2,分子数减少,即分子总数小于0.5NA,故A错误;
B.双氧水和水都含有氧原子,25g质量分数68%的H2O2水溶液中含氧原子数目大于NA,故B错误;
C.n=$\frac{m}{M}$计算得到物质的量=$\frac{16.8g}{56g/mol}$=0.3mol,结合铁和水蒸气反应生成四氧化三铁和氢气计算电子转移数,3Fe~Fe3O4~8e-,则Fe与足量水蒸气完全反应失去0.8NA个电子,故C正确;
D.一个CH5+含有的电子数为10,1 mol CH5+含有的电子数目为10NA,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,题目难度不大,熟练掌握公式的使用和物质的结构是解题关键.


科目:高中化学 来源: 题型:实验题
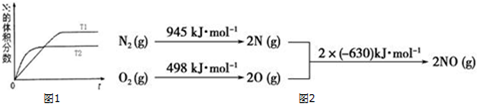
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
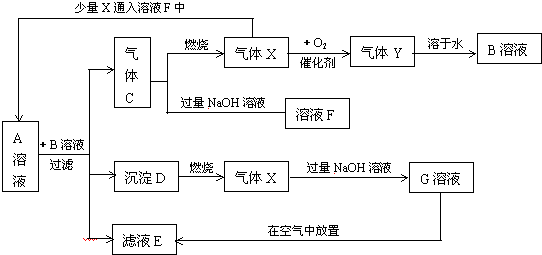
| A. | 气体C是SO2 | |
| B. | 溶液A和溶液B可能的化学反应为3Na2S+Na2SO3+4H2SO4=3S↓+H2S↑+4Na2SO4+3H2O | |
| C. | 若氧气足量气体C可以一步反应得到气体Y | |
| D. | 图中少量X通入溶液F中不涉及氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
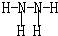
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高 | |
| B. | 乙醇依次通过消去、取代、加成反应可生成乙二醇 | |
| C. | 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | |
| D. | 等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++4 NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 18gD2O中含有的中子数为10 NA(设NA为阿伏加德罗常数的数值) | |
| C. | 明矾既可以用于净水,又可杀菌消毒 | |
| D. | 恒温恒容下,某可逆反应X(g)+Y(g)?Z(g)+W(s)△H>0达平衡后再加入X,该反应的△H不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 .
.
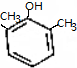 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
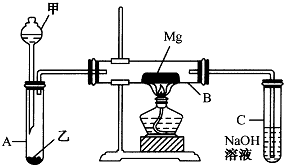 已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com