
已知:
(1)试分析说明这个总反应的实际价值和意义.
(2)在实现这一总反应的过程中,对中间产物进行甲烷的发酵研究,做了下同位素示踪实验:

在同样的反应条件下,请预测下列反应产物:
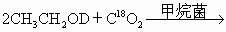
|
(1) 利用秸杆、杂草、树叶等农作物的废弃物在甲烷菌催化作用后便有沼气产生,它是农村能源的一种重要来源,也是扩大肥源、提高肥效和改善农村环境卫生的重要措施.(2) |
|
(1) 从化学视角来审视反应物 ,其应为纤维素.秸杆、杂草、树叶等农作物的废弃物,在农村来源充足,而且有利于改善农村的环境卫生.另一方面,产物甲烷是一种优质燃料,可作为农村日常生活的重要能源.农村开发沼气前景广阔,具有良好的经济效益和社会效益;(2)根据题给同位素示踪实验反应式,可得出反应规律:每两分子的醇和 ,其应为纤维素.秸杆、杂草、树叶等农作物的废弃物,在农村来源充足,而且有利于改善农村的环境卫生.另一方面,产物甲烷是一种优质燃料,可作为农村日常生活的重要能源.农村开发沼气前景广阔,具有良好的经济效益和社会效益;(2)根据题给同位素示踪实验反应式,可得出反应规律:每两分子的醇和 反应,生成两分子的羧酸和甲烷,其中醇分子中羟基氢和.碳原子上的氢原子转移到二氧化碳分子中而形成产物甲烷分子.依此规律进行推理不难得出答案. 反应,生成两分子的羧酸和甲烷,其中醇分子中羟基氢和.碳原子上的氢原子转移到二氧化碳分子中而形成产物甲烷分子.依此规律进行推理不难得出答案. |


科目:高中化学 来源: 题型:阅读理解
| 物 质 | 熔点(℃) | 沸点(℃) | 密度(g/cm3) |
| 乙 醇 | -117.0 | 78.0 | 0.79 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | - | 338.0 | 1.84 |
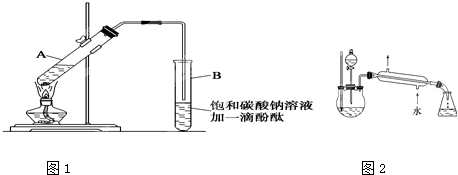
 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O查看答案和解析>>
科目:高中化学 来源: 题型:
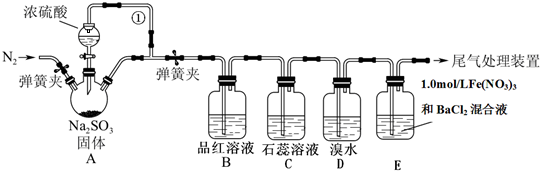
查看答案和解析>>
科目:高中化学 来源: 题型:038
已知:
(1)试分析说明这个总反应的实际价值和意义.
(2)在实现这一总反应的过程中,对中间产物进行甲烷的发酵研究,做了下同位素示踪实验:

在同样的反应条件下,请预测下列反应产物:
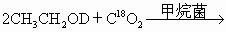
查看答案和解析>>
科目:高中化学 来源:2011年高考化学一轮复习:《饮食中的有机化合物》(解析版) 题型:解答题
| 物 质 | 熔点(℃) | 沸点(℃) | 密度(g/cm3) |
| 乙 醇 | -117.0 | 78.0 | 0.79 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | - | 338.0 | 1.84 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com