
| A、相同 | B、中和盐酸的多 |
| C、中和醋酸的多 | D、无法比较 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、任何能使熵值增大的过程都能自发进行 |
| B、已知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-QkJ?mol-1(Q>0),则将2molSO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出QkJ的热量 |
| C、化学平衡发生移动,平衡常数一定发生变化 |
| D、足量的锌粒分别和等体积同浓度的CH3COOH、HCl反应,两者放出氢气质量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧燃料电池在碱性介质中的正极反应式为:O2+2H2O+4e-═4OH- | ||||
B、用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1-+2H2O
| ||||
| C、粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu2++2e-═Cu | ||||
| D、钢铁发生电化学腐蚀的负极反应式为:Fe-2e-═Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C(H+)=10-3mol/L |
| B、C(OH-)=10-9mol/L |
| C、pH=4 |
| D、溶液中由水电离的C(H+)=10-10mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
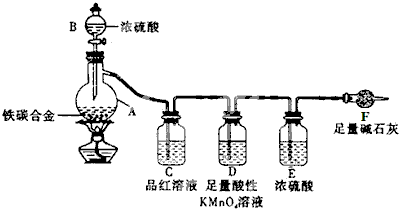
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合物 | A | B | C |
| 结构简式 |  | 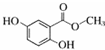 | 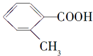 |
| 化合物 | D | E | F |
| 结构简式 | 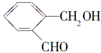 | 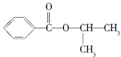 | 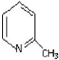 |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com