
【题目】下列反应符合图示的是( ) 
A.红热的炭与水蒸气反应制取水煤气
B.锌与稀硫酸的反应
C.酸碱中和反应
D.二氧化硫的催化氧化反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,又是一种可再生能源,具有广泛的开发和应用前景。
(1)已知反应CO(g)+2H2(g) ![]() CH3OH(g)H=-99kJ.mol-1中的相关化学键键能如下:
CH3OH(g)H=-99kJ.mol-1中的相关化学键键能如下: 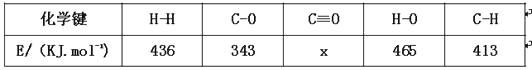
则x=。
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g) ![]() CH3OH(g) H1<0,CO在不同温度下的平衡转化率(α)与压
CH3OH(g) H1<0,CO在不同温度下的平衡转化率(α)与压
强的关系如下图所示。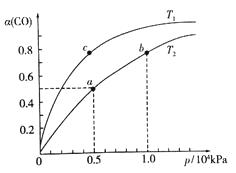
①a、b两点的反应速率:v(a)v(b)(填“>”“<”或“=”)。
②T1T2(填“>”“<”或“=”),原因是。
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
④图中a点的平衡常数KP=(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)利用合成气(主要成分为CO和H2)合成甲醇,发生主要反应如下:I:CO(g)+2H2(g) ![]() CH3OH(g) H1II:CO2(g)+H2(g)
CH3OH(g) H1II:CO2(g)+H2(g) ![]() CO(g) + H2O(g) H2III:CO2(g)+3H2(g)
CO(g) + H2O(g) H2III:CO2(g)+3H2(g) ![]() CH3OH(g) + H2O(g) H3
CH3OH(g) + H2O(g) H3
上述反应对应的平衡常数分别为K1、K2、K3 , 它们随温度变化曲线如下图所示。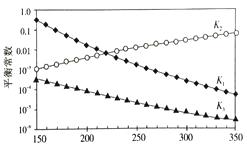
则H1H3(填“>”、“<”、“=”), 理由是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A元素原子的L电子层比B元素原子的L电子层少3个电子,B元素原子核外总电子数比A 元素原子电子总数多5个,则A、B形成化合物可能是
A. 离子化合物ABB. 离子化合物B3A2
C. 离子化合物B2(AO3)3D. 离子化合物A2BO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质特征是
A. 胶体粒子直径在1-100nm之间 B. 胶体粒子带电荷
C. 胶体粒子不能穿过半透膜 D. 胶体粒子能够发生布朗运动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一位同学为探究元素周期表中元素性质的递变规律,设计了如下列实验.
(1)根据题意解答 (i)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:与盐酸反应最剧烈,与盐酸反应的速度最慢;与盐酸反应产生的气体最多.
(ii)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为 .
(2)利用如图装置可验证同主族元素非金属性的变化规律: 
(i)仪器B的名称为 , 干燥管D的作用为 .
(ii)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液的现象,即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用溶液吸收尾气.
(iii)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有溶液的洗气瓶除去.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于氧化还原反应的是( )
A.2KI+Br2═2KBr+I2
B.CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
C.SO3+H2O ![]() H2SO4
H2SO4
D.MgCl2+2NaOH ![]() Mg(OH)2↓+NaCl
Mg(OH)2↓+NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是部分短周期元素主要化合价与原子序数的关系图,下列说法不正确的是( ) 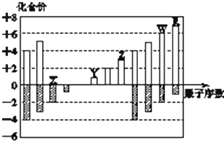
A.X和W位于同一主族
B.原子半径:Y>Z>X
C.盐YRX与化合物WX2的漂白原理相同
D.Y和R两者的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.0mL 0.10molL﹣1的NaOH溶液中逐滴加入0.10molL﹣1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( ) 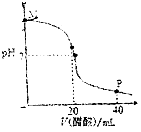
A.N点处恰好完全反应,c(CH3COO﹣)=c(CH3COOH)
B.O点处显中性,c(CH3COO﹣)=c(Na+)=c(H+)=c(OH﹣)
C.M点到O点过程中,可能出现c(CH3COO﹣)>c(Na+)
D.P点处显酸性,c(CH3COO﹣)+c(CH3COOH)=2c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com