
| A.W1>W2>W3 | B.W1=W2=W3 |
| C.W3>W1>W2 | D.W3>W2>W1 |
科目:高中化学 来源:不详 题型:计算题
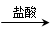 测得生成气体的体积Vml(已折算成标准状况);
测得生成气体的体积Vml(已折算成标准状况); 测得剩余固体的质量a克;
测得剩余固体的质量a克;  溶液
溶液 测得沉淀的质量b克。
测得沉淀的质量b克。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1︰2 | B.1︰3 | C.3︰2 | D.1︰1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
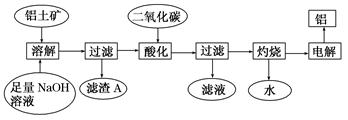
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,含有杂质
,含有杂质 、
、 、
、 。工业上从铝土矿中提取铝可采用如下工艺流程:
。工业上从铝土矿中提取铝可采用如下工艺流程: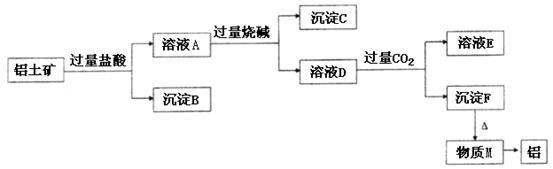
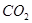 生成沉淀F的离子方程式为________________________。
生成沉淀F的离子方程式为________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
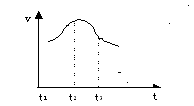
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
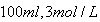 的盐酸和
的盐酸和 溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为( )
溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为( )| A.5.4g | B.3.6 g | C.2.7 g | D.1.8 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
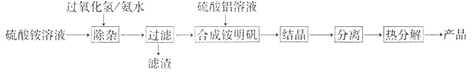
| A.蒸馏 | B.分液 | C.过滤 | D.洗涤晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com