
氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
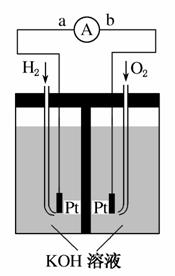
(1)氢氧燃料电池的能量转化主要形式是________________,在导线中电子流动方向为________(用a、b表示)。
(2)负极反应式为___________________________________。
(3)电极表面镀铂粉的原因为_________________________。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2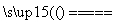 2LiH
2LiH
Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是________,反应Ⅱ中的氧化剂是________。
②已知LiH固体密度为0.82 g/cm3,用锂吸收224 L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为________。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为________mol。
科目:高中化学 来源: 题型:
现通过以下具体步骤由制取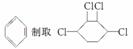
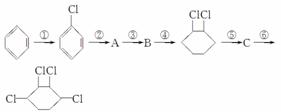
(1)从左到右依次填写每步反应所属的反应类型(只填字母):a.取代反应,b.加成反应,c.消去反应,d.加聚反应。
①________;②________;③________;④________;
⑤________;⑥________。
(2)写出①、⑤、⑥三步反应的化学方程式:
①________________________________________________________________________;
⑤________________________________________________________________________;
⑥________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质或离子检验的叙述正确的是
A、 在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B、 气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气
C、 灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+
D、 将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。
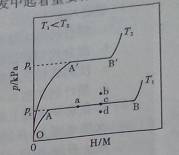
在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐惭增大;在AB段,MHx与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)==ZMHy(s) △H(Ⅰ);在B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。反应(Ⅰ)中z=_____(用含x和y的代数式表示)。温度为T1时,2g某合金4min内吸收氢气240mL,吸氢速率v=______mL•g-1•min。反应的焓变△HⅠ_____0(填“>”“<”或“=”)。
(2)η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)____ η(T2)(填“>”“<”或“=”)。当反应(Ⅰ)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应(Ⅰ)可能处于图中的_____点(填“b”“c”或“d”),该贮氢合金可通过______或_______的方式释放氢气。
(3)贮氢合金ThNi5可催化由CO、H2合成CH4的反应,温度为T时,该反应的热化学方程式为_________。已知温度为T时:CH4(g)+2H2O=CO2(g)+4H2(g) △H=+165KJ•mol
CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41KJ•mol
查看答案和解析>>
科目:高中化学 来源: 题型:
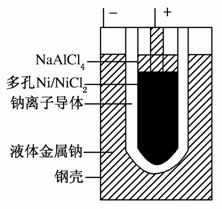
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是( )
A.水既是氧化剂又是溶剂
B.放电时正极上有氢气生成
C.放电时OH-向正极移动
D.总反应为:2Li+2H2O===2LiOH+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案,不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 检验食盐中是否添加KIO3 | 取食盐试样,溶于KI溶液,加入淀淀溶液,观察溶液是否变蓝 |
| B | 验证硝酸是挥发性酸 | 用两根玻璃棒分别蘸取浓硝酸和浓氨水,然后靠近,观察是否有白烟产生 |
| C | 验证Br2氧化性强于Fe3+ | 取少许FeCl2晶体溶于稀盐酸,加入KSCN观察溶液是否变红,滴入溴水后再观察是否变红 |
| D | 检验氯酸钾中含有氯元素 | 取少量氯酸钾加入MnO2充分加热,残留物溶于水,取上层清液,滴入硝酸酸化的AgNO3溶液,观察是否有白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是

A.b>f
B.平衡常数K(1000℃)<K(810℃)
C.915℃,2.0MPa该反应的平衡常数为Kp=4.5MPa
D.1000℃,3.0MPa时E的转化率为83%
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W有如图所示的转化关系,则X、Y可能是
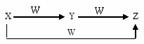 ①C 、CO ② S、SO2
①C 、CO ② S、SO2
③ AlCl3、Al(OH)3 ④Cl2、FeCl3
A.仅有①③ B.①②③
C.仅有②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是( )。
A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH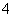 )之和
)之和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com