
| A. | SO2、H2S、Cl2 | B. | SO2、O2、NH3 | C. | NO、O2、H2 | D. | SO2、CO2、O2 |
分析 在通常状况下能共存,说明气体相互之间不反应,浓硫酸具有酸性和氧化性,不能干燥碱性和还原性气体,据此分析解答.
解答 解:A.硫化氢具有还原性,能够与浓硫酸反应,不能用浓硫酸干燥,故A错误;
B.氨气为碱性气体,能够与浓硫酸反应,不能用浓硫酸干燥,故B错误;
C.一氧化氮与氧气常温下反应生成二氧化氮,不能共存,故C错误;
D.二氧化硫、二氧化碳、氧气相互不反应,且都与浓硫酸不反应,能够用浓硫酸干燥,故D正确;
故选D.
点评 本题考查了物质的共存与浓硫酸的干燥性,熟悉相关气体性质及浓硫酸的性质是解题关键,注意浓硫酸具有酸性和氧化性,不能干燥碱性和还原性气体,侧重考查学生对基础知识掌握熟练程度.


科目:高中化学 来源: 题型:选择题
| A. | CO2 H2O | B. | NH3 BCl3 | C. | PCl3 CH4 | D. | PCl5 CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100ml 2mol/LFeCl3溶液 | B. | 75ml 1mol/LMgCl2溶液 | ||
| C. | 150ml 3mol/LKCl溶液 | D. | 25ml 2mol/LAlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2+Cl2$\frac{\underline{\;光照\;}}{\;}$2HCl | B. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | ||
| C. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | D. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Cl2>I2 | B. | SiCl4>CCl4 | ||
| C. | NH3>PH3 | D. | C(CH3)4>CH3CH2CH2CH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢离子在银表面被还原,产生气泡 | B. | 银片质量逐渐增大 | ||
| C. | 电子从锌片经导线流向银片 | D. | 锌是负极,其质量逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
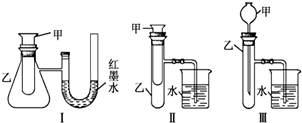
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
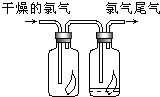 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com