

| 物质 | 性质(沸点及分解温度均为101kPa测得) |
| 邻苯二甲酸酐 (M=148g/mol) | 白色针状晶体.不溶于冷水,溶于热水及有机溶剂. 密度1.53g/cm3,沸点295℃. |
| 正丁醇(M=74g/mol) | 无色液体.微溶于水,溶于有机溶剂.密度0.81g/cm3,沸点117.7℃.可与水形成二元共沸物(沸点92.7℃). |
| 邻苯二甲酸二丁酯 (M=278g/mol) | 无色油状液体.难溶于水,溶于有机溶剂.密度1.49g/cm3,沸点340℃.酸性条件下180℃以上易发生分解. |
 转变成盐,从而与产物分离,该操作是否可改用NaOH溶液?否(填“是”或“否”),原因是;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;.加入食盐水洗涤一方面是防止有机物发生乳化而不利于分层,另一方面是为了降低邻苯二甲酸二丁酯的溶解度.
转变成盐,从而与产物分离,该操作是否可改用NaOH溶液?否(填“是”或“否”),原因是;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;.加入食盐水洗涤一方面是防止有机物发生乳化而不利于分层,另一方面是为了降低邻苯二甲酸二丁酯的溶解度.分析 (1)依据装置图和仪器的用途分析回答仪器名称;浓硫酸在反应中起到催化作用,吸水剂;用减压蒸馏的目的是减压蒸馏可降低有机物的沸点;
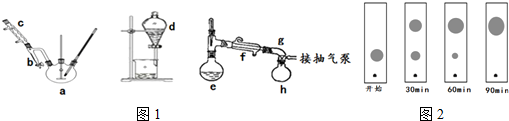
(2)冷凝管应从下口进水,上口出水;根据分水器中的水位不再发生变化,说明反应结束;
(3)碳酸钠溶液洗涤的目的是用碳酸钠除去酯中的硫酸和 ;根据氢氧化钠碱性较强,能使邻苯二甲酸二丁酯发生水解;邻苯二甲酸二丁酯在盐溶液中溶解度会降低;
;根据氢氧化钠碱性较强,能使邻苯二甲酸二丁酯发生水解;邻苯二甲酸二丁酯在盐溶液中溶解度会降低;
(4)对照图上的斑点分析,可以知道,反应开始时图上的斑点是反应物,由此可推知,回流30min、60min时的图上,下面的斑点为反应物,上面的斑点为生成物,90min时则图上的斑点是生成物,而反应物基本上无剩余,但不会消失;
解答 解:(1)蒸馏时使用的仪器e的名称蒸馏烧瓶;浓硫酸在反应中起到催化作用,吸水剂,加快化学反应速率,促使平衡正向移动;用减压蒸馏的目的是减压蒸馏可降低有机物的沸点,可以防止有机物脱水碳化,提高产物的纯度;
故答案为:蒸馏烧瓶;催化剂,吸水剂;可降低有机物的沸点,可以防止有机物脱水碳化,提高产物的纯度;
(2)冷凝管应从下口进水,上口出水,则制备装置中冷凝水的流向与冷凝管中蒸汽的流向相同,根据分水器中的水位不再发生变化,说明反应结束;
故答案为:相同;分水器中的水位不再发生变化;
(3)产品纯化过程中,加入Na2CO3溶液的目的是使硫酸和 转变成盐,从而与产物分离;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;邻苯二甲酸二丁酯在盐溶液中溶解度会降低,所以加入食盐水洗涤一方面是防止有机物发生乳化而不利于分层,另一方面是为了降低邻苯二甲酸二丁酯的溶解度;
转变成盐,从而与产物分离;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;邻苯二甲酸二丁酯在盐溶液中溶解度会降低,所以加入食盐水洗涤一方面是防止有机物发生乳化而不利于分层,另一方面是为了降低邻苯二甲酸二丁酯的溶解度;
故答案为:将硫酸和 转变成盐,从而与产物分离;否;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;降低邻苯二甲酸二丁酯的溶解度;
转变成盐,从而与产物分离;否;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;降低邻苯二甲酸二丁酯的溶解度;
(4)对照图上的斑点分析,可以知道,反应开始时图上的斑点是反应物,由此可推知,回流30min、60min时的图上,下面的斑点为反应物,上面的斑点为生成物,90min时则图上的斑点是生成物,而反应物基本上无剩余,但不会消失,因此,不可能出现的情况是D;
故选:D.
点评 本题以物质的制备为背景,考查蒸馏、分液等基本操作,掌握实验操作的要求和实验原理是解题的关键,难度较大.


科目:高中化学 来源: 题型:解答题
| 实验编号 | a | b | c |
| 样品质量(g) | 9.6 | 12.8 | 64.0 |
| 气体体积(L) | 5.04 | 6.72 | V |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某研究小组探究:
某研究小组探究:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>HBr>HI | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H2SO4 | D. | 熔点:SiO2>NaCl>CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
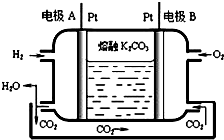 运用所学化学原理,解决下列问题:
运用所学化学原理,解决下列问题:| 温度/ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钙的元素符号:Ca | B. | 硫离子结构示意图: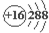 | ||
| C. | 二氧化碳的结构式 O=C=O | D. | NaCl的电子式: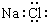 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com