
| A. | 若a>b,一定存在c(A-)=c(K+) | B. | 若a=2b,一定存在c(A-)>c(K+) | ||
| C. | 若2a=b,一定存在c(OH-)>c(A-) | D. | 若a=b,一定存在c(OH-)=c(H+)+c(HA) |
分析 常温下PH=2的一元酸HA中,c(H+)=0.01mol/L,PH=12的KOH溶液c(H+)=10-12mol/L,c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-12}}$mol/L=0.01mol/L,等体积混合,所得溶液显酸性,HA是弱酸,现将amol/LHA bmol/LKOH等体积混合,a=b,溶液显碱性,a=2b,溶液中为等物质的量的钾盐和弱酸,若电离大于水解呈酸性,反之呈碱性,所以a>b,溶液显酸性或碱性,若2a=b,溶液一定呈碱性,结合原子守恒、电荷守恒分析各选项.
解答 解:常温下PH=2的一元酸HA中,c(H+)=0.01mol/L,PH=12的KOH溶液c(H+)=10-12mol/L,c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-12}}$mol/L=0.01mol/L,等体积混合,所得溶液显酸性,HA是弱酸.
A.将amol/LHA bmol/LKOH等体积混合,若a>b,酸过量,若过量的酸的电离大于其生成的钾盐的水解程度,导致溶液中,c(H+)>c(OH-),根据电荷守恒c (A-)+c (OH-)=c(K+)+c(H+),则c(A-)>c(K+),故A错误;
B.将amol/LHA bmol/LKOH等体积混合,a=2b,溶液中为等物质的量的钾盐和弱酸,若电离大于水解呈酸性,c(H+)>c(OH-),根据电荷守恒c (A-)+c (OH-)=c(K+)+c(H+),则c(A-)>c(K+),若水解大于电离,则溶液呈碱性,c(H+)<c(OH-),根据电荷守恒c (A-)+c (OH-)=c(K+)+c(H+),则c(A-)<c(K+),故B错误;
C.将amol/LHA bmol/LKOH等体积混合,若2a=b,溶液中为等物质的量的钾盐和KOH,钾盐水解,氢氧化钾完全电离,一定存在c(OH-)>c(A-),故C正确;
D.将amol/LHA bmol/LKOH等体积混合,若a=b,若等物质的量浓度等体积的一元酸碱混合溶液,二者恰好反应生成KA盐,因HA是弱酸,A-水解,所以c(K+)=c (A-)+c(HA)①,溶液中存在电荷守恒c (A-)+c (OH-)=c(K+)+c(H+)②,将①代入②得:c(OH-)=c(H+)+c(HA),故D正确;
故选CD.
点评 本题考查离子浓度大小比较及酸碱强弱的定性判断,题目难度中等,注意盐的水解原理和实质,易错选项是B,明确溶液酸性原因是解答关键.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHC2O4溶液(pH=5.5):c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) | |
| B. | 向NaHCO3溶液中通CO2至pH=7:c(Na+)=c(HCO3-)+2c(CO32-) | |
| C. | 向NaHSO4溶液中加入等浓度等体积的Ba(OH)2溶液:pH=13 | |
| D. | 向氨水中加入少量NH4Cl固体:$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
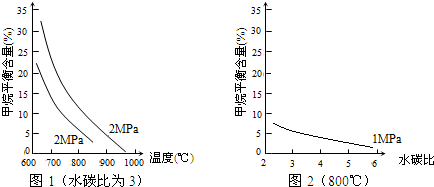
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中的二氧化碳接触,生成 了乳白色的凝胶状沉淀(用H2SiO3表示)和碳酸钠的缘故 | |
| B. | 水的物理性质十分特殊.水的比热容较大,水结成冰后密度变小,水的熔沸点较高等特殊 性质是由于水分子间存在一种被称为氢键的特殊的分子间作用力 | |
| C. | 铅蓄电池是最常见的二次电池,由于它的性能优良、价格低廉、安全可靠,可多次充放电,所以使用广泛,但铅蓄电池也存在比能量低,废弃电池污染环境等缺点 | |
| D. | 硅晶体是一种重要的半导体材料,在常温下,单质硅易与氧气反应,所以自然界中不存在 游离态的硅.石墨烯作为目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材 料,最有潜力的应用是成为硅的替代品,用来生产未来的超级计算机 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素均可与氢元素形成 18电子分子 | |
| B. | X、Y、Z、W形成的单质最多有 6种 | |
| C. | 四种元素中,Z的最高价氧化物对应水化物酸性最强 | |
| D. | 四种元素的原子半径:rZ>rX>rY>rW |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| B. | 聚乙炔用I2或Na等做掺杂处理后可形成一种导电塑料,该导电塑料是一种纯净物 | |
| C. | 用蘸有浓氨水的棉棒检验输送氯气的管道是否漏气 | |
| D. | 用合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
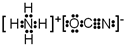 或
或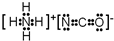 .
.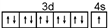 .A、B元素形成的最简单的化合物不能与E2+形成配合物的原因是CH4不能提供孤对电子.
.A、B元素形成的最简单的化合物不能与E2+形成配合物的原因是CH4不能提供孤对电子. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,78g Na2O2的分子数为NA | |
| B. | 标准状况下,22.4L氯气在任何反应中转移电子数均为2NA | |
| C. | 标准状况下,22.4mL H2O中含水分子的个数约为1.24NA | |
| D. | 17g NH3溶于水后溶质NH3的个数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com