
【题目】已知:
2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;
Na2O2(s)+CO2(g)=Na2CO3(s)+ ![]() O2(g)△H=﹣226kJ/mol
O2(g)△H=﹣226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
B.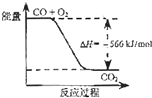
如图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>﹣452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
【答案】C
【解析】解:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出热量;已知:2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;一氧化碳的燃烧热为283KJ/mol;故A错误;
B、依据热化学方程式,2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;分析图象中一氧化碳和氧气物质的量为1、 ![]() 物质的量不符合反应物质的物质的量;故B错误;
物质的量不符合反应物质的物质的量;故B错误;
C、固体二氧化碳变化为气体二氧化碳需要吸热,焓变放热是负值;依据热化学方程式判断,2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=﹣226kJ/mol;所以反应
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H>﹣452 kJ/mol,故C正确;
D、已知:
①2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;
②Na2O2(s)+CO2(g)=Na2CO3(s)+ ![]() O2(g)△H=﹣226kJ/mol
O2(g)△H=﹣226kJ/mol
依据盖斯定律②×2+①得到:2Na2O2(s)+2CO(g)=2Na2CO3(s)△H=﹣1018KJ/mol;
即Na2O2(s)+CO(g)=Na2CO3(s)△H=﹣509KJ/mol;
CO(g)与Na2O2(s)反应放出509 kJ热量时,反应的一氧化碳物质的量为1mol,电子转移数为2×6.02×1023 , 故D错误;
故选C.
A、依据燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出热量;
B、依据热化学方程式,2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;分析图象中物质的量不符合反应物质物质的量;
C、固体二氧化碳变化为气体二氧化碳需要吸热,焓变放热是负值;
D、依据热化学方程式,结合盖斯定律计算得到热化学方程式计算分析;


科目:高中化学 来源: 题型:
【题目】把一定量的Na2O2和NaHCO3的混合粉末分为两等份,将其中一份加入到100mL稀盐酸中恰好完全反应,生成的气体干燥后体积为2.24L(标况);再将此气体通入另一份混合物中,恰好完全反应后,得到O2 2.016L(标况),则加入稀盐酸的物质的量浓度是( )
A.3.4mol/L
B.0.2mol/L
C.1.8mol/L
D.3.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按要求填空:
①第三周期中有两个成单电子的元素符号是________;
②四核10电子的粒子的电子式(写一种)__________;
③第四周期中,3d轨道半充满的元素符号是________________。
(2)下列物质中:①白磷(P4) ②水晶 ③氯化铵 ④氢氧化钙 ⑤氟化钠 ⑥过氧化钠 ⑦石墨,固态下都为晶体,回答下列问题(填写序号):
不含金属离子的离子晶体是________,只含离子键的离子晶体是________,既有离子键又有非极性键的离子晶体是________,既有离子键又有极性键的离子晶体是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.吸热反应不加热一定不能发生
C.放热的反应在常温下一定很容易发生
D.反应是放热还是吸热须看反应物和生成物所具有的总能量的相对大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( ) 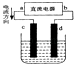
A.a为负极、b为正极
B.d为阳极,电极反应为:2Cl﹣﹣2e﹣=Cl2↑
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气、一氧化碳、辛烷、甲烷燃烧的热化学方程式分别为: H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.8kJ/mol
O2(g)=H2O(l)△H=﹣285.8kJ/mol
CO(g)+ ![]() O2(g)=CO2(g)△H=﹣282.6kJ/mol
O2(g)=CO2(g)△H=﹣282.6kJ/mol
C8H18(l)+ ![]() O2(g)=8CO2(g)+9H2O(l)△H=﹣5472kJ/mol
O2(g)=8CO2(g)+9H2O(l)△H=﹣5472kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=﹣889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( )
A.H2(g)
B.CO(g)
C.C8H18(l)
D.CH4(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化工生产不符合实际的是
A. 海水提溴时用到热空气将Br2吹出
B. 工业制HCl时氯气在氢气中燃烧
C. 将氯气通入石灰乳中制取漂粉精
D. 钠在氯气中燃烧生产氯化钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com