
| A、向AgCl悬浊液中加入足量的NaI溶液,无明显现象 |
| B、CCl4和NH3两分子各原子最外层均满足8电子结构 |
| C、若短周期R2+和M+的电子层结构相同,则金属性R>M |
| D、硝酸铵溶于水吸热,是焓减熵增的过程 |


科目:高中化学 来源: 题型:
| A、FeCl3溶液、Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是有没有丁达尔现象 |
| B、按反应物与生成物种类的多少把所有的无机反应分为分解反应、复分解反应、置换反应与化合反应 |
| C、HCl(强电解质)、CH3COOH(弱电解质)、CH3I(非电解质)、CO2(电解质) |
| D、研究物质的性质一般按观察物理性质、预测化学性质、验证或探究物质的性质与分析现象并解释这四个步骤进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
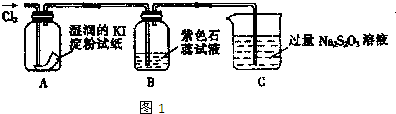
| ||
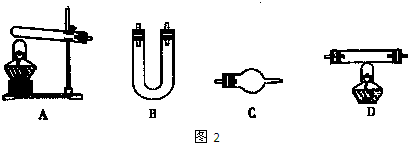
| 选用的仪器(填字母) | 加入的试剂 | 作用 |
| 反应器(或产生气体) | ||
| 氧化铜 | 使氨气与氧化铜反应 | |
| C |
查看答案和解析>>
科目:高中化学 来源: 题型:
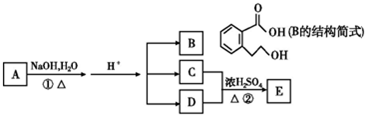
查看答案和解析>>
科目:高中化学 来源: 题型:
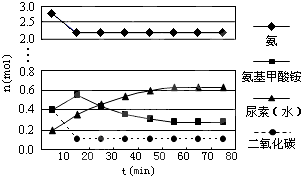
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、-1641.0kJ/mol |
| B、+3081kJ/mol |
| C、+663.5kJ/mol |
| D、-2507.0kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、46 | B、61.3 |
| C、76.7 | D、69 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com