
【题目】80℃时,2 L密闭容器中充入0.40 mol N2O4,发生如下反应:N2O4(g)![]() 2NO2(g)。一段时间后达到平衡,测得数据如下:
2NO2(g)。一段时间后达到平衡,测得数据如下:
时间/s | 20 | 40 | 60 | 80 | 100 |
c(NO2)/( mol·L1) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
请回答:
(1)20 s内,v(NO2) =_________mol/(L·s) 1。
(2)升高温度时,c(NO2)增大,则正反应是______(选填“放热”或“吸热”)反应。
(3)该温度下反应的化学平衡常数数值为______。
(4)该条件下N2O4的平衡转化率是______。
科目:高中化学 来源: 题型:
【题目】右图为原电池示意图,回答下列问题:
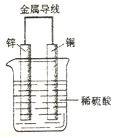
(1)该装置能够将_________能转化成电能。
(2)锌是原电池的_______极,放电过程中____(填“得”或“失”)电子,发生_______反应。
(3)电子是由_______极通过导线流向________极。
(4)铜电极的电极的反应式为____________________
(5)总反应的化学方程式为_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 增加气体反应物浓度,单位体积内活化分子数增加,活化分子百分数增加,有效碰撞次数增加,所以反应速率加快
B. 镁与稀盐酸反应时,加入适量的氯化钾溶液,生成氢气的速率不变
C. 对于可逆反应,升高反应体系温度,正反应速率和逆反应速率均增加
D. 在密闭容器中发生反应 A(g)+B(g)![]() C(g)+D(g),保持恒温恒容,充入气体 He 增大压强,化学反应速率加快
C(g)+D(g),保持恒温恒容,充入气体 He 增大压强,化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收。已知X是化石燃料燃烧产物之一,是形成酸雨的主要物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应。请写出下列物质反应的化学方程式。
(1)X在一定条件下与氧气反应____________________________________;
(2)Y与氢氧化钠溶液的反应______________________________________;
(3)Z与水的反应________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从石油中裂解获得 A 是目前工业上生产A的主要途径,图中的 N 是高分子化合物。以 A 和 1,3 一丁二烯为原料合成 N 的流程如下:

(1)D 物质的名称为_____;B→C 的化学反应方程式为_____________。
(2)G 中含氧官能团的名称为_____________,由 G→H 的反应类型为_________。
(3)在催化剂存在下,E 和 M 等物质的量发生聚合反应,N 的结构简式为__________。
(4)E 有多种同分异构体,符合下列条件的同分异构体最多有______种。
①可与 Na2CO3 溶液反应;②分子中只有一个环状结构。
(5)天然橡胶是异戊二烯的聚合物,其单体是 CH2=C(CH3)CH=CH2。试以异戊二烯为原料(其他无机试剂任选),设计制备 的合成路线,请写出合成路线流程图_____。
的合成路线,请写出合成路线流程图_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,固定容器中,无论以何比例混合,其密度都不变的是
A. CH4 和 C2H4 B. C3H6和 CO2
C. C2H6和 C2H4 D. CO和C2H4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com