
分析 根据原子或者分子:核外电子数=质子数;
阳离子:核外电子数=质子数-所带电荷数;
阴离子:核外电子数=质子数+所带电荷数.
解答 解:原子或者分子:核外电子数=质子数;
阳离子:核外电子数=质子数-所带电荷数;
阴离子:核外电子数=质子数+所带电荷数.
(1)核外电子总数为2的原子为He,离子为Li+,分子为H2,故答案为:He,Li+,H2等;
(2)核外电子总数为10的粒子原子为Ne,离子为Na+,分子为HF等,故答案为:Ne,Na+,HF等;
(3)核外电子总数为18的粒子原子为Ar,离子为K+,分子为HCl等,故答案为:Ar,K+,HCl等.
点评 本题考查粒子核外电子数的计算,注意原子或者分子:核外电子数=质子数;阳离子:核外电子数=质子数-所带电荷数;阴离子:核外电子数=质子数+所带电荷数,难度不大.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:解答题
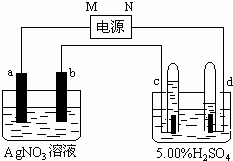 如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体.请回答下列问题.
如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,8 g CH4含有4NA个氢原子 | |
| B. | 2gD216O中含有的质子数为2NA个 | |
| C. | 1 mol Cu与足量FeCl3溶液反应,转移2NA个电子 | |
| D. | 通常状况下,2.24 L氮气含有0.1NA个N2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
时间 (s)浓度 mol•L-1 | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | C1 | 0.10 | C3 | C4 | C5 |
| C(NO2) | 0.00 | 0.12 | C2 | 0.22 | 0.22 | 0.22 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
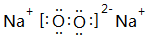 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com