
 计算空气的物质的量,再根据N=nNA计算气体分子数目;
计算空气的物质的量,再根据N=nNA计算气体分子数目;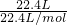 =1mol,含有气体分子数目为1mol×NAmol-1=NA,故B正确;
=1mol,含有气体分子数目为1mol×NAmol-1=NA,故B正确;

 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:
设![]() 为阿伏伽德罗常数的值,下列叙述正确的是
为阿伏伽德罗常数的值,下列叙述正确的是
A.标准状态下,33.6L氟化氢中含有氟原子的数目为![]()
B.常温常压下,7.0g乙烯与丙稀的混合物红含有氢原子的数目为![]()
C.50mL18.4![]() 浓硫酸与足量铜微热反应,生成
浓硫酸与足量铜微热反应,生成![]() 分支的数目为0.46
分支的数目为0.46![]() 。
。
D.某密闭容器盛有0.1mol![]() 和0.3mol
和0.3mol![]() ,在一定条件下充分反应,转移电子的数目为0.6
,在一定条件下充分反应,转移电子的数目为0.6![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
设![]() 为阿伏伽德罗常数的值,下列叙述正确的是
为阿伏伽德罗常数的值,下列叙述正确的是
A.常温下, 的
的 溶液中氮原子数为0.2
溶液中氮原子数为0.2![]()
B.1 羟基中电子数为10
羟基中电子数为10
C.在反应 中,每生成3
中,每生成3
![]() 转移的电子数为6
转移的电子数为6![]()
D.常温常压下,22.4L乙烯中![]() 键数为4
键数为4![]()
查看答案和解析>>
科目:高中化学 来源:2010年江苏高考真题 题型:单选题
设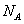 为阿伏伽德罗常数的值,下列叙述正确的是
为阿伏伽德罗常数的值,下列叙述正确的是
A.常温下,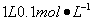 的
的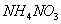 溶液中氮原子数为0.2
溶液中氮原子数为0.2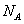
B.1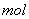 羟基中电子数为10
羟基中电子数为10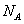
C.在反应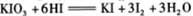 中,每生成3
中,每生成3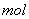
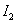 转移的电子数为6
转移的电子数为6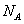
D.常温常压下,22.4L乙烯中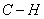 键数为4
键数为4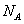
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com