
X��Y��Z��W��ԭ��������������Ķ�����Ԫ�أ��һ���ͬ�壻����ֻ������Ϊ������Xԭ�ӵ������������������������ȣ�X��W��Y��Z������ԭ�ӵ�����������֮�;�Ϊ9������Y��W������Ũ��NaOH��Һ��Ӧ������˵������ȷ����
A�����Ӱ뾶�� Z>W >Y B���ǽ�������ǿ��Ԫ��ΪW
C��Y������������Ӧ��ˮ����Ϊ���� D��XW2�����ӻ�����
D
��������
��������������������֪X��Be��Y��Al��Z��S��W��Cl��A�����ڵ��Ӳ�ṹ��ͬ��������˵��ԭ������Խ�����Ӱ뾶��ԽС�����ڵ��Ӳ�ṹ��ͬ��������˵�����Ӻ�����Ӳ���Խ�࣬���Ӱ뾶��Խ���������Ӱ뾶�� Z>W >Y����ȷ��B��ͬһ���ڵ�Ԫ�أ�ԭ������Խ��Ԫ�صķǽ����Ծ�Խǿ�������ڵ���������ԭ������������Cl�����Էǽ�������ǿ��Ԫ��ΪW����ȷ��C��Y��Al�����ڴ��ڽ�����ǽ����Ľ�����������������������Ӧ��ˮ����Ϊ���ԣ���ȷ��D��XW2�ǹ��ۻ��������
���㣺����Ԫ�ص��ƶϡ�Ԫ�����ڱ���Ԫ�������ɵ�֪ʶ��Ӧ�á�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ��ɽ�и�����һ�ε����о��������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
�����±��ṩ��ʵ�����ĺ�ҩƷ�����ܴﵽ��Ӧʵ��Ŀ�ĵ���
��� | ʵ������ | ʵ��ҩƷ | ʵ��Ŀ�� |
A | ������ƽ�������룩��100mL����ƿ����Ͳ���ձ���ҩ�ס������� | NaCl���塢����ˮ | ����100 mLһ�����ʵ���Ũ�ȵ�NaCl��Һ |
B | ���Թܡ�����©�����п����ϰ塢���ܼ���Ƥ��������ƿ������Ƭ����� | ϡ���ᡢ��״ʯ��ʯ | ��ȡ���ռ�������̼���� |
C | ��ʽ�ζ��ܡ���ʽ�ζ��ܡ���ͷ�ιܡ�����̨�������У�����ƿ | ��֪Ũ�ȵ�NaOH��Һ���������ᡢ����ˮ����ֽ | �ⶨϡ��������ʵ���Ũ�� |
D | ����̨�������У����ƾ��ơ����Թܡ�����ƿ�����ܼ���Ƥ�� | �Ȼ�� | ��ȡ���ռ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�����и�����ѧ�ڽ��Ŀ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��51.2 g Cu��ȫ��������Ũ�����У��ռ��������������NO��N2O4��NO2���Ļ���ﹲ0.8mol����Щ����ǡ���ܱ�500 mL NaOH��Һ��ȫ���գ�����NaNO2��NaNO3��������Һ������NaNO3�����ʵ���Ϊ0.2 mol����NaOH��Ũ��Ϊ
A��2mol/L B��1.8mol/L C��2.4 mol/L D��3.6 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�����и�����ѧ�ڽ��Ŀ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
A3+��������46�����ӣ�������Ϊ115����Aԭ�Ӻ������������
A��66 B��46 C��115 D��49
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ������ѧ��12���¿����ۻ�ѧ�Ծ���A���������棩 ���ͣ������
��8�֣�PM2.5��������������Ӱ�������������������Ⱦ�����Ҫ��ԴΪȼú��������β���ȡ���ˣ���PM2.5��SO2��NOx �Ƚ����о�������Ҫ���塣��ش��������⣺
��1����PM2.5����������ˮ�����Ƴɴ�����������ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���
���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
Ũ��/mol?L-1 | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
���ݱ��������ж�PM2.5������pH ��
��2��NOx ����β������Ҫ��Ⱦ��֮һ����������������ʱ������N2��O2��Ӧ���������仯ʾ��ͼ���£�

��N2��O2��Ӧ����NO���Ȼ�ѧ��Ӧ����ʽΪ
��3����ѭ�����ղ���������SO2���ͻ�����Ⱦ��ͬʱ�����Ƶ������������������£�

�������ӷ���ʽ��ʾ��Ӧ���з����ķ�Ӧ��
�ڽ����ɵ������������ֱ�ͨ����������Ե缫��KOH��Һ��Ϊ�������Һ�������ĵ缫��Ӧʽ_ _
��10�֣���Ԫ������Ȼ������Ҫ��������������Ҫ�ɷ�ΪAl2O3��������Fe2O3��FeO��SiO2���С���ҵ�����������Ʊ�����ij�ֻ�����Ĺ����������¡�

����ҺA�м���Ư��Һ��Ŀ��������������������ҺB�����ԡ�
��1��������ҺB���Ƿ�����Ԫ�صķ���Ϊ�� ��ע���Լ�������
��2������ҺB�е���Ԫ���Գ�����ʽ��������ѡ�õ�����Լ�Ϊ ������ţ���
A������������Һ B��������Һ C����ˮ D��������̼
��3������ҺB�Ʊ��Ȼ��������漰�IJ���Ϊ�� ����Ũ������ȴ�ᾧ�� ��ϴ�ӡ�
��4��SiO2��NaOH�����Ʊ������ƣ��ɲ��õ�װ��Ϊ ������ţ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ��һ12���¿���ѧ�Ծ��������棩 ���ͣ������
(22��)�������о������ʣ�
��H2 ���� ��CuO ��CO2 ��H2SO4 ��Ba(OH)2���� �߰�ˮ ��ϡ���� ������Al2(SO4)3
��1�������ʵķ������д����Ŀհ״���
����� | �ܵ��� | �ǵ���� | ����� |
���ڸ�������� |
��2��������������������������֮��ɷ������ӷ�Ӧ��H����OH��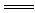 H2O�������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽΪ ��
H2O�������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽΪ ��
��3������ˮ�еĵ��뷽��ʽΪ ��
34.2g������ˮ���250mL��Һ�� SO42-�����ʵ���Ũ��Ϊ ��
��4�������Ģ�ͨ�����Һ�з�Ӧ�����ӷ���ʽΪ: ��
��5�����ڼ���NaOH����Һ�з�Ӧ�����ӷ���ʽ
��6����������Ӧ�Ļ�ѧ����ʽΪ��Al + 4HNO3 = Al(NO3)3 + NO�� + 2H2O���÷�Ӧ����������
���ѧʽ������ԭ���������������ʵ���֮���� ������5.4g Al������Ӧʱ��ת�Ƶ��ӵ����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ��һ12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���;�ˮ����������أ�K2FeO4��Ϊ����ɫ���壬������ˮ����ҵ���Ʊ�K2FeO4�ij��÷���֮һ�Ǵ�����������������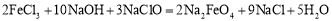
��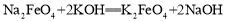 ������˵������ȷ����
������˵������ȷ����
A����Ӧ��Ϊ������ԭ��Ӧ����Ӧ��Ϊ���ֽⷴӦ
B����Ӧ�������������뻹ԭ�������ʵ���֮��Ϊ2:9
C����Ӧ�ڵIJ���K2FeO4��FeΪ+6�ۣ�����ǿ�����ԣ���ɱ������
D������2mol FeCl3������Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ6 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ijѧ���������ǵ�ˮ��ʵ�飬������ˮ��������Ƿ��������ǡ����IJ������£�ȡ���������Ǽ������Һ����������Һ�м���3��5��ϡ��������Һ��м����ӡ���ȴ������ȴ�����Һ�м�����������ˮԡ�м��ȡ�ʵ����û��������������ԭ����
A��������δˮ�� B������ˮ��IJ�����û��������
C������ʱ�䲻�� D����к����Һ��û�мӼ���к�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪:������Ũ��Ϊ0.1 mol��L-1��������Һ��pH���:
���� | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
�����й�˵����ȷ����
A������ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳��H2CO3��HClO��HF
B������CO2 ͨ��0.1 mol��L-1Na2CO3��Һ������Һ���ԣ�����Һ��2 c (CO32��)+ c (HCO3��)= 0.1 mol��L-1
C�������ϱ�, ˮ�ⷽ��ʽClO��+ H2O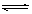 HClO + OH����ƽ�ⳣ��K��10��7.6
HClO + OH����ƽ�ⳣ��K��10��7.6
D��������NaClO ��Һ��ͨHF������ǡ����ȫ��Ӧʱ��c(Na+)��c(F��)��c(H+)��c(HClO)��c(OH��)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com