
| A、①③ | B、①④ | C、②③ | D、②④ |


科目:高中化学 来源: 题型:
| A、过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体 |
| B、过氧乙酸与苯酚混合使用,可增强过氧乙酸杀菌效果 |
C、由下列过氧乙酸的制取原理可以看出,过氧乙酸是酯的同系物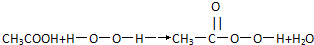 |
| D、浓过氧乙酸溶液中加入少许紫色石蕊试液,振荡后先变红,后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO2 |
| B、NO |
| C、N2O |
| D、N2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
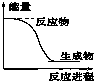
| A、碳与二氧化碳化合成为一氧化碳 |
| B、HCl分解为H2和Cl2 |
| C、Na与H2O反应 |
| D、Ba(OH)2?8H2O和NH4Cl晶体混合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、催化剂能降低正反应的活化能,但不能改变逆反应的活化能 |
| B、在稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| C、由C(石墨)→C(金刚石);△H=+73 kJ/mol,可知金刚石比石墨稳定 |
| D、在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、13C与14C互为同位素,化学性质相同,但相对原子质量一定不同 |
| B、某元素原子次外层电子数是最外层电子数的2倍,则该元素氧化物为酸性氧化物 |
| C、IA族元素与VIIA元素形成的化合物都为离子化合物 |
| D、短周期中,同周期元素的离子半径从左到右逐渐减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L乙烯含有的极性共价键数为NA |
| B、常温下,5.6LNO和5.6LO2的混合气体中含有的分子数为0.5NA |
| C、16.9gBaO2固体中阴、阳离子总数为0.2NA. |
| D、常温常压下,28g氮气含有的核外电子数为10 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com