
分析 (1)利用太阳能分解海水是将太阳能转化为化学能;氢氧燃料电池属于原电池,是将化学能转化为电能,断裂化学键需要吸收能量,形成化学键放出能量;
(2)原电池中,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流出;
(3)(a)锌片、银片、稀硫酸构成原电池,活泼金属锌作负极,负极上失电子发生氧化反应,银作正极,正极上得电子发生还原反应,据此写出电极反应式;
(b)根据得失电子守恒计算生成氢气的体积.
解答 解:(1)科学家利用太阳能使海水分解,所以是太阳能转变为化学能,该反应中二氧化钛作催化剂;生成的氢气用于燃料电池时是把化学能转变为电能,水分解时,断裂的化学键是H-O键;电解水是吸热反应,
故答案为:催化剂、化学、电、吸热;
(2)A极是失去电子发生氧化反应的电极,所以A极是负极,正极上得电子发生还原反应,所以电子从负极流出,故答案为:负;流出;
(3)(a)锌片、银片、稀硫酸构成原电池,锌作负极,负极上锌失电子发生氧化反应,电极反应式为:Zn-2e-=Zn2+;银作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,
故答案为:Zn-2e-=Zn2+;2H++2e-=H2↑;
(b)该原电池中,负极上锌失电子变成锌离子进入溶液,导致质量减少,正极上金属不参加反应,所以该装置中减少的质量是锌的质量,根据转移电子相等知,生成氢气的物质的量和锌的物质的量相等,所以生成气体的体积=$\frac{(60-47)g}{65g/mol}$×22.4L/mol=4.48L,所以参加反应锌的质量为
$\frac{4.48}{22.4}×65$g=13g,故答案为:4.48L,13g.
点评 本题考查原电池反应的原理,负极发生氧化反应,正极发生还原反应,在得失电子守恒的情况下根据电极反应进行计算,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
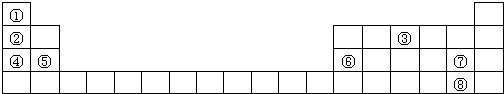
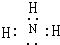 ,实验室制取该氢化物的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
,实验室制取该氢化物的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②③⑤ | C. | ①③ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 可被酸性高锰酸钾溶液氧化为
可被酸性高锰酸钾溶液氧化为 (苯甲酸),但若烷基R中直接与苯环相连接的碳原子上没有C-H键,则不容易被氧化得到苯甲酸.据此判断,分子式为C11H16的一烷基取代苯,可以被氧化为苯甲酸的异构体共有( )
(苯甲酸),但若烷基R中直接与苯环相连接的碳原子上没有C-H键,则不容易被氧化得到苯甲酸.据此判断,分子式为C11H16的一烷基取代苯,可以被氧化为苯甲酸的异构体共有( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有③ | B. | ③④⑤ | C. | ②④⑤⑥ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、I2、HI共存 | |
| B. | 单位时间内生成n mol H2,同时生成n mol I2 | |
| C. | 单位时间内生成2n mol HI,同时生成n mol I2 | |
| D. | H2、I2、HI的 物质的量浓度比为1:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6gCH4中含有的电子数 | |
| B. | 100mL1mol/LH2SO4中含有H+的数 | |
| C. | 24gMg与足量稀盐酸反应转移的电子数 | |
| D. | 标准状况下,22.4LCO气体中含有的原子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2(g)=$\frac{1}{2}$O2(g)=H2O(I)△H>-241.8kJ•mol-1 | |
| B. | H2的燃烧热△H=-241.8 kJ.mol-1 | |
| C. | H2(g)转变成H2O(g)的化学反应一定放出能量 | |
| D. | CO(g)+H2O(g)=CO2(g)+H2(g)的△H=-41.2kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com